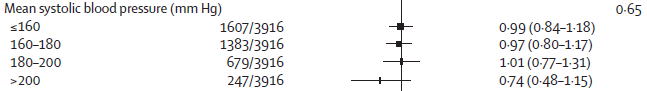�@�z�[���@���@�Ȃ낭�@��
�Ȃ낭�|��������
�@�������f�ÃK�C�h���C��
 ACP/AAFP����ҍ��������ÃK�C�h���C���@�i���ڐV��2017/1/17�j ACP/AAFP����ҍ��������ÃK�C�h���C���@�i���ڐV��2017/1/17�j
 �iAnn Intern Med. 2017�j �iAnn Intern Med. 2017�j
2017�N1��17���CACP�i�č����Ȋw��j��AAFP�i�č��ƒ��w��j������҂̍��������Âɂ��Ă̐f�ÃK�C�h���C���\���܂����DGRADE system�ɏ������Ă��܂��D��{�I��JNC8�Ɩ������܂���D
�ȉ��C���̓��e�����܂��D
ACP�^AAFP����ҍ��������ÃK�C�h���C���������e
60�Έȏ㐬�l�ɂ����鍂�������ÖڕW
����1
ACP��AAFP��60�Έȏ㐬�l�����k�������������I��150 mmHg�ȏ�ł���Ύ��S�C�]�����C�S�C�x���g�̃��X�N�����炷���߂�150 mmHg������ڕW�Ɏ��Â��J�n���邱�Ƃ𐄏�����i�O���[�h�F���������C�������̃G�r�f���X�j�DACP��AAFP�͗Տ��Ƃ�60�Έȏ�̐��l�̎��ÖڕW��I�Ԃ̂ɁC����̌����ڕW�̗��v�ƊQ�̋c�_�����҂ƂƂ��ɒf���I�ɍs�����Ƃ𐄏�����D
����2
ACP��AAFP�͔]������TIA�̊����̂���60�Έȏ㐬�l���]�����̍Ĕ��̃��X�N�����炷���߂Ɏ��k�������̖ڕW��140 mmHg�����ɂ���悤�ɖÖ@���J�n���������邱�Ƃ�Տ��Ƃ��l�����邱�Ƃ����߂�i�O���[�h�F�ア�����C�����x�̎��̃G�r�f���X�j�DACP��AAFP�͗Տ��Ƃ�60�Έȏ�̐��l�̎��ÖڕW��I�Ԃ̂ɁC����̌����ڕW�̗��v�ƊQ�̋c�_�����҂ƂƂ��ɒf���I�ɍs�����Ƃ𐄏�����D
����3
ACP��AAFP�͌ʉ����ꂽ�]���Ɋ�Â��S���ǃ��X�N�̍���60�Έȏ㐬�l���]������S���ǃC�x���g�̃��X�N�����炷���߂Ɏ��k�������̖ڕW��140
mmHg�����ɂ���悤�ɖÖ@���J�n���������邱�Ƃ�Տ��Ƃ��l�����邱�Ƃ����߂�i�O���[�h�F�ア�����C�Ⴂ���̃G�r�f���X�j�DACP��AAFP�͗Տ��Ƃ�60�Έȏ�̐��l�̎��ÖڕW��I�Ԃ̂ɁC����̌����ڕW�̗��v�ƊQ�̋c�_�����҂ƂƂ��ɒf���I�ɍs�����Ƃ𐄏�����D |
 JNC 8�iEighth Joint National Committee�j�@�i���ڐV��2014/1/14�C�ŏI�X�V2014/3/16�j JNC 8�iEighth Joint National Committee�j�@�i���ڐV��2014/1/14�C�ŏI�X�V2014/3/16�j
 �iJAMA. 2014;311(5):507-520�j �iJAMA. 2014;311(5):507-520�j
2013�N12��18���CNHLBI�i�č��S�x���nj������j�̓K�C�h���C���Q��1�ł�����10�N�Ԃ�̉���ɂȂ鍂�����f�ÃK�C�h���C���CJNC 8�i�č������������ψ����8���j�\���܂����D
�ȉ��C���̓��e�����܂��D
JNC 8�������e
�������Ǘ��̐����iJNC8�j
����1
60�Έȏ�̈�ʓI�ȏW�c�ł́C�~���̂��߂̖��Â����k�������iSBP�j��150mmHg���g���������iDBP�j��90mmHg�ŊJ�n���CSBP��150mmHg����DBP��90mmHg��ڕW�Ƃ��Ď��Â���i��������
- Grade A�j�D
�K�R�I�Ȑ���
60�Έȏ�̈�ʓI�ȏW�c�ł́C�������ɑ�����Â��ڕWSBP��艺����Ă��āi�Ⴆ��140mmHg�j�C�F�e���������C���N��QOL�ɑ��镛��p���Ȃ��Ȃ�C���Â͒��߂���i�킴�킴�グ��j�K�v�͂Ȃ��i���Ƃ̈ӌ� - Grade E�j�D
����2
60�Ζ����̈�ʓI�ȏW�c�ł́C�~���̂��߂̖��Â�DBP��90mmHg�ŊJ�n���CDBP��90mmHg��ڕW�Ƃ��Ď��Â���i30�`59�F��������
- Grade A�C18�`29�F���Ƃ̈ӌ� - Grade E�j�D
����3
60�Ζ����̈�ʓI�ȏW�c�ł́C�~���̂��߂̖Ö@��SBP��140mmHg�ŊJ�n���CSBP��140mmHg��ڕW�Ƃ��Ď��Â���i���Ƃ̈ӌ�
- Grade E�j�D
����4
18�Έȏ�̖����t���a�iCKD�j�̏W�c�ł́C�~���̂��߂̖��Â����k�������iSBP�j��140mmHg���g���������iDBP�j��90mmHg�ŊJ�n���CSBP��140mmHg����DBP��90mmHg��ڕW�Ƃ��Ď��Â���i���Ƃ̈ӌ�
- Grade E�j�D
����5
18�Έȏ�̓��A�a�̏W�c�ł́C�~���̂��߂̖��Â����k�������iSBP�j��140mmHg���g���������iDBP�j��90mmHg�ŊJ�n���CSBP��140mmHg����DBP��90mmHg��ڕW�Ƃ��Ď��Â���i���Ƃ̈ӌ�
- Grade E�j�D
����6
��ʓI�Ȕl�̏W�c�ł́C���A�a���܂݁C�~�����Â̑��I���̓T�C�A�U�C�h�n���A�܁C�J���V�E���h�R��iCCB�j�C�A���M�I�e���V���ϊ��y�f�j�Q�܁iACEI�j�C�A���M�I�e���V����e�̎Ւf��iARB�j�̂����ꂩ�ɂ���ׂ��ł���i�����x�̐���
- Grade B�j�D
����7
��ʓI�ȍ��l�̏W�c�ł́C���A�a���܂݁C�~�����Â̑��I���̓T�C�A�U�C�h�n���A�܂��J���V�E���h�R��iCCB�j�̂����ꂩ�ɂ���ׂ��ł���i��ʓI�ȍ��l�W�c�F�����x�̐���
- Grade B�C���A�a�̍��l���ҁF�ア���� - Grade C�j�D
����8
18�Έȏ��CKD�W�c�ł́C�~�����Â̑��I���i���邢�͏�悹�j�ɂ́C�t�A�E�g�J�������P�����邽�߂�ACEI��ARB���܂߂�ׂ��ł���D����͐l��ⓜ�A�a�̏�ԂɊW�Ȃ��C�S�Ă̍���������CKD���҂ɓK�p����i�����x�̐���
- Grade B�j�D
����9
���������Â̎�ȖړI�́C�����̖ڕW�l�ɒB���Ă�����ێ����邱�Ƃł���D����1�����ȓ��ɖڕW�����ɓ��B���Ȃ��Ȃ�C�ŏ��̖�܂̗ʂ𑝂₷���C����6�̃N���X�i�T�C�A�U�C�h�n���A�܁CCCB�CACEI�CARB�j�̂�����1���2�I���Ƃ��ĉ�����D�Տ��Ƃ͌����̕]�����p�����C�ڕW�����ɒB����܂ŁC���Ó��e�߂���D2�ܗp���Ă��ڕW�����ɒB���邱�Ƃ��ł��Ȃ��ꍇ�́C����ɂ��̒�����3�ܖڂ�������������DACEI��ARB�����҂ŕ��p���Ă͂Ȃ�Ȃ��D�֊�����������C�ڕW�����ɓ��B����̂�3�܂��z���Ďg�p���Ȃ���Ȃ�Ȃ����߂ɁC����6�̖�܂����ł͖ڕW�����ɒB���邱�Ƃ��ł��Ȃ��ꍇ�́C���̃N���X�̍~���܂�p���邱�Ƃ��ł���D��L�̐헪��p���Ă��~���ڕW�ɒB���Ȃ����҂�C�lj��̗Տ��I�ȃR���T���e�[�V�������K�v�Ȃ悤�ȍ����ǂ����������҂̊Ǘ��̂��߂ɂ́C����������ւ̏Љ�K���ɂȂ邾�낤�i���Ƃ̈ӌ�
- Grade E�j�D
|
�����̍����ƂȂ�_���Əؖ�����Ă�����ʁi�{������쐬�j
| ���� |
���� |
���p���� |
���p���ꂽ�����̖��O |
�ؖ�����Ă������ |
| ����1 |
60�Έȏ� |
6�� |
HYVET�CSyst-Eur�CSHEP�CJATOS�CVALISH�CCARDIO-SIS |
�]�����C�S�s�S�C�����������iCHD�j |
| ����2 |
60�����C
�g�������� |
5�� |
HDFP�CHypertension-Stroke Cooperative�CMRC�CANBP�CVA Cooperative |
�]���ǎ����C�S�s�S�C�����S |
| ����3 |
60�����C
���k������ |
0�� |
|
|
| ����4 |
CKD |
3�� |
AASK�CMDRD�CREIN-2 |
GFR�CESRD�ւ̐i�W�C�S���ǎ��� |
| ����5 |
���A�a |
3�� |
SHEP�CSyst-Eur�CUKPDS |
�����S�C�S���ǎ����C�]���ǎ����C�t���a�i�C�S�s�S�͂Ȃ��j |
| ����6 |
�l��ܑI�� |
3�� |
VA Cooperative Trial�CHDFP�CSHEP |
�S���ǎ����C�]���ǎ����C���S |
| ����7 |
���l��ܑI�� |
1�� |
ALLHAT |
�S���ǎ����C�S�s�S�C�����S���ǃA�E�g�J�� |
| ����8 |
CKD��ܑI�� |
2�� |
IDNT�CAASK |
�S�s�S�C�t���a |
| ����9 |
��ܒlj� |
0�� |
|
|
�G�r�f���X�Ɋ�Â����~���܂̓��^�ʁiTable 4�����ρj
| �~���܁i���{�̐攭�i���i���j |
����1��
���^��(mg) |
���r���[���ꂽRCT�ł�
�ڕW���^��(mg) |
1��
����� |
�i�Q�l�j���{�ł�
�Y�t�������^�� |
ACE�j�Q�܁iACEI�j
�@Captopril�i�J�v�g�v�����j
�@Enalapril�i���j�x�[�X�j
�@Lisinopril�i�����Q�X�j |
50
5
10 |
150-200
20
40 |
2
1-2
1 |
37.5�`75mg3�~�C�ő�150mg
5�`10mg1�~
10�`20mg1�~ |
�A���M�I�e���V����e�̎Ւf�܁iARB�j
�@Eprosartan�i���{�������j
�@Candesartan�i�u���v���X�j
�@Losartan�i�j���[���^���j
�@Valsartan�i�f�B�I�o���j
�@Irbesartan�i�A�o�v���C�C���x�^���j |
400
4
30
40-80
75 |
600-800
12-32
100
160-320
300 |
1-2
1
1-2
1
1 |
4�`8mg1�~�C�ő�12mg
25�`50mg1�~�C�ő�100mg
40�`80mg1�~�C�ő�160mg
50�`100mg1�~�C�ő�200mg
|
���Ւf�܁iBB�j
�@Atenolol�i�e�m�[�~���j
�@Metprolol�i�Z���P��L�j |
25-50
50 |
100
100-200 |
1
1-2 |
50mg1�~�C�ő�100mg
120mg1�~ |
�J���V�E���h�R�܁iCCB�j
�@Amlodipine�i�A�����W���C�m���o�X�N�j
�@Diltiazem extended release�i�w���x�b�T�[R�j
�@Nitrendipine�i�o�C���e���V���j |
2.5
120-180
10 |
10
360
20 |
1
1
1-2 |
2.5�`5mg�C�ő�10mg
100�`200mg1�~
5�`10mg1�~ |
�T�C�A�U�C�h�n���A��
�@Bendroflumethiazide�i���{�������j
�@Chlorthalidone�i���{�������j
�@Hydrochlorothiazide�i�q�h���N�����`�A�W�h�F�攭�i�������~�j
�@Indapamide�i�i�g���b�N�X�j |
5
12.5
12.5-25
1.25 |
10
12.5-25
25-100a
1.25-2.5 |
1
1
1-2
1 |
25�`100mg1�`2�~
2mg1�~ |
a���݂̐�������Ă�����ʂƈ��S���̃o�����X�ɂ����ăG�r�f���X�Ɋ�Â������^�ʂ́C25-50mg/���ł���D
�����̃|�C���g�ƍl�@
�����Ɋւ���ő�̃|�C���g�́C����҂ƁC�S�N��̓��A�a���҂�CKD���҂ł́C�~���ڕW��10mmHg���オ���ĊÂ��Ȃ������Ƃ��������܂��i���A�a��CKD�̂Ȃ���N�҂ł͈ȑO���140/80mmHg�����ŕς�炸�j�D���̌��ʁC����܂ł̓��{�̍������f�ÃK�C�h���C���̊Ǘ��ڕW�����Â��Ȃ��Ă��܂��D
�����C�S�̓I�Ɍ��āC�����x�͐��Ƃ̈ӌ��ł���GRADE E���قƂ�ǂŁC���m�ȃG�r�f���X���Ȃ����Ƃ�������܂��D�������Ƃ�����r�I�G�r�f���X���L�x�Ȏ����ł����Ă��C�~���������������Ƃ������Ƃ͌����Ă��C��̓I�ɁC�ǂ���g���āC�ǂ̒��x������̂��������ɂ��ẴG�r�f���X�͕s�\���Ȃ̂ł��D����́C���A�a�⎉���ُ�ǂȂǁC���̎����ł������邱�Ƃł��D���������āC�K�������f�ÃK�C�h���C���̐����ʂ莡�Â��Ȃ���Ȃ�Ȃ����̂ł͂���܂���D
���{�������w��̌��s�̍������f�ÃK�C�h���C���i���������ÃK�C�h���C��2009�j�́C2014�N4�������������ÃK�C�h���C���iJSH2014�j�ɉ��������\��ł��D���ꂽ���̊T�v�i�L���v�`���摜�j�ɂ��ƁC��36����{�������w���̓��ʊ��u���������ÃK�C�h���C��JSH2014�T�v�v�ɂ����ĉ����_��������܂����D���I�����Ւf����O���CCCB�CARB�CACEI�C���A���4�N���X�Ƃ����\��Ƃ��Ă��܂��D�����JNC 8�Ɠ����ł��D�������CARB��ACEI�Ɣ�r���Č��ʂ������`������ɖ��������Ƃ���C���I���Ƃ��邱�Ƃ͓K���ł͂���܂��C���K�C�h���C���Ƃ�����ɂ��Ă͐G��Ă��܂���D
�~���ڕW�ɂ��āC�����[�����Ƃ�����܂��D60�Έȏ�̊��҂ɂ�����~���ڕW��150/90mmHg�����ɂ���Ƃ�������1�̍����Ƃ��āC6����RCT���������Ă��܂����C���̂������ʂɎ��k��������140mmHg�����ɂ��邱�Ƃ��C��荂��140�`160mmHg��140�`149mmHg�ɂ��邱�ƂƔ�r���Ēlj��̗��v���Ȃ��Ƃ�����{�̌����iJATOS: Hypertens Res 2008;31:2115�CVALISH: Hypertension 2010;56:196�j�����p����Ă��܂��D�l��▯���̈Ⴂ����C�C�O�̐f�ÃK�C�h���C����a��̂ł̓_���ŁC���{�l�̃G�r�f���X�܂������{�Ǝ��̐f�ÃK�C�h���C�����K�v���Ƃ���ӌ���p�ɂɎ��ɂ��܂����C���{�ł̌����̐��ʂ��ނ�����{�̐f�ÃK�C�h���C���Ŋ������Ă��Ȃ��Ƃ����̂́C�Ȃ�Ƃ�����ł��D�~���ڕW�͂����ƊÂ��Ă����Ǝv���܂��D�l�I�ɂ́C����҂�60�Έȏ�ňꊇ��ɂ���̂ɂ͒�R������C�N��オ��ɘA��Č������㏸���Ă����Ƃ������R�o�߂��l�����āC�����Ƃ��܂߂ɁC����ɍ~���ڕW���������Ă����ėǂ��Ǝv���̂ł��D
����2�Ŏ�����Ă���60�Ζ����̊g���������̖ڕW�����ɂ��ẮCHOT trial�iLancet 1998;351:1755�j��80mmHg�����C85mmHg�����C90mmHg�����̔�r�ŗ��v�ɈႢ���Ȃ��������߁C90mmHg�����̐����ɂȂ�܂����D
����3�̍����ƂȂ�RCT���Ȃ��Ƃ����̂͋����ł����C60�Ζ����ł͊g���������̌�����90mmHg�����̌Q�̎��k�������T��140mmHg�������̂ŁC���Ƃ̈ӌ���140mmHg�����̐����ɂȂ����Ƃ̂��Ƃł��D�g���������̕������d������Ă���Ƃ����܂��D
����4�̐������K�p�����̂́C70�Ζ����̗\���܂��͑��肳�ꂽGFR��60mL/min/1.73m2�̊��ҌQ�ƁC������GFR�̑S�N��̃A���u�~���A��30mg/gCr��L���銳�ҌQ�ł��D������C130/80mmHg�����ɂ��邱�Ƃ�140/90mmHg�����ɂ�������t���a��S���ǎ����̃G���h�|�C���g��L�ӂɌ��炷�Ƃ������ʂ͌�������܂���ł����D�܂��C70�Έȏ��CKD���҂ɂ�����ڕW�����ɂ��ẴG�r�f���X�͂Ȃ��C�ʂɍl����ׂ����Ƃ���Ă��܂��D
����5�ɂ��ẮC���A�a���҂ɂ����āC���k��������150mmHg��������140mmHg�����ɂ������������b�g������Ƃ���RCT�͑��݂��܂���DACCORD-BP
trialT�iN Engl J Med 2010;362:1575�j�ł��C140mmHg�����Ƃ���ȉ��̃R���g���[�����r���ėL�ӂȍ����݂�ꂸ�C140mmHg�̐������x�����Ă��܂��D�匌�ǃC�x���g�ƍ����ǃC�x���g��������ADVANCE
trial�iLancet 2007;370:829�j�ł́C�Ⴂ�����ɂ���ċt��CVD���X�N���㏸���邱�Ƃ�������܂����D�������C���̌����͑g�ݓ���̍ۂ̃x�[�X���C���̌��������߂��Ă��炸�C�܂������_�����t������Ă��Ȃ��������߁C����̃G�r�f���X���r���[�ł͍̗p����܂���ł����D
����6�̃��Ւf�����I������O���ꂽ�����Ƃ��ẮC���Ւf��ARB�����]�������ǂ𑝂₵���Ƃ���LIFE trial�iLancet 2002;359:995�j�����p����Ă��܂��D���Ւf�����I���Ƃ��ėp���邱�Ƃɂ��ẮC���A�܂Ɣ�r���ĐS���ǎ����C�S�s�S�C�����S���ǃA�E�g�J��������������Ƃ���ALLHAT�iHypetension 2003;42:239�j�������ɁC�O����܂����D�܂������Ւf��icarvedilol�j�C���NJg���^���Ւf��inebivolol�j�C��������2�����_�o�쓮��iclonidine�j�C���ڌ��NJg����ihydralazine�j�C�A���h�X�e������e�̝h�R��ispironolactone�j�C�����������_�o�쓮��ireserpine�j�C���[�v���A��ifurosemide�j�ɂ��Ă͎���good��fiar��RCT�����݂��Ȃ��������߁C���I���O����܂����D����ɁC���A�܂�ARB���r����RCT�ƁCACEI��ARB���r����RCT�͂���܂���ł����D�܂��CACEI��ARB�̕��p���ʂ�������ONTARGET�́C���������҈ȊO���g�ݍ��܂�Ă����̂ŁC����̃G�r�f���X���r���[�ł͍̗p����܂���ł����D
���̐����ɂ��Ă̏d�v�ȃ|�C���g��4����Ɩ{�����ɏ�����Ă��܂��D1�Ԗڂ́C�����̊��҂ō~���܂͕����̎g�p���K�v�ŁC���̐����͑��I���̑I���ɂ̂ݓK�p�����̂ł���C�p�l���Ƃ��Ă�4�̃N���X�̂ǂ��lj������܂Ƃ��ėp���Ă��ǂ��ƒ�Ă��܂��D2�Ԗڂ́C���̐�����thiazide�Cchlorthalidone�Cindapamide�Ƃ������T�C�A�U�C�h�n���A��ɓ��ʂȂ��̂ł���C���[�v���A���J���E���ێ������A�܂͊܂܂�Ă��܂���D3�Ԗڂ́CRCT�Ŏ����ꂽ���l�Ȍ��ʂ邽�߂Ɋe��܂͏\���ʓ��^����邱�Ƃ��d�v�ł��iTable 4�j�D4�Ԗڂ́C������������S�s�S�Ȃǂ̍����ǂ�������������łȂ�����̏W�c��ΏۂƂ���RCT�́C���̐����ł̓��r���[����Ă��Ȃ��̂ŁC�����̏W�c�ɓK�p����ۂɂ͒��ӂ���ׂ��ł��D
���ʓI�ɃT�C�A�U�C�h�n���A�܁CCCB�CACEI�CARB��4�܂����I���Ƃ���Ă��܂����C���̂���ARB�͍ł��������C����ACEI�Ɣ�r��������ACEI������ʂ��������G�r�f���X���F���ł��邱�Ƃ���C���I���Ƃ��Ă͕s�K���ƍl�����܂��D������ACEI�Ɣ�r����ARB�̕����F�e�����������Ƃ������b�g�Ƃ��ċ������Ă��܂��D���̏ꍇ�̔F�e���Ƃ́CACEI�ɂ���P�̕���p���w���Ă��܂����CACEI�g�p�҂̂����C�j����1���C������3�����x�̔��Ǘ��ł���C�قƂ�ǂ�����J�n�̏����ɋN����C�x���P���������邱�Ƃ���C�܂�ACEI���g�p���Ă݂āC��P���o��悤�Ȃ�ARB�ւ̕ύX�����������Ƃ����l�����̕����Ó��ł��D��������ƁC�����đ��I���Ƃ͂Ȃ蓾�܂���D�~���܂ōł�����グ���グ�Ă���̂�ARB�ł����C�������I���ɂ���̂���߂邱�ƂŁC��Ô���Ȃ�}���ł���ƍl����܂��D
����7��ALLHAT�̃T�u��́iJAMA 2002;288:2981�j�������ɂȂ��Ă��܂��D���̃T�u��͂ł́C���l�ł�ACEI�Ɣ�r���ė��A�܂��g�p���������S���ǎ����C�S�s�S�C�����S���ǃA�E�g�J���ɂ��L���ł����DCCB�͗��A�܂Ɣ�r���ĐS�s�S�̗\�h�Ɍ��ʂ����܂������C���̃A�E�g�J���ɗL�ӂȍ����Ȃ����Ƃ���C���l�̍������̑��I���Ƃ��Đ�������Ă��܂��D
����8��CKD���҂ɑ��ẮCIDNT�iN Engl J Med 2001;345:851�j�̌��ʂŁCARB��CCB�����S�s�S�����P�������Ƃ�ACEI/ARB�����I���ɂȂ��Ă��܂����C���̌����͂Ƃ��̂��a���t�ǂŒ`���A������W�c�Ɍ��肳��Ă��܂����D���̐�����18�Έȏ�ɓK������܂����C75�Έȏ�ł̃G�r�f���X������܂���D���������āC75�Έȏ�ł́C�T�C�A�U�C�h�n���A���CCB���I�����Ƃ��ċ������܂��D
JNC 8��JSH2014�̑���_�́C�ƒ댌���̈����ɂ�����܂��DJSH2014�͉ƒ댌�����d�����C�u�f�@�������Ɖƒ댌���̊Ԃɐf�f�̍�������ꍇ�C�ƒ댌���ɂ��f�f��D�悷��v�Ƃ��܂����D�܂��C�����̑���ɂ��āu����2�肵�C���̕��ϒl�v�Ɩ��L���Ă��܂��D����CJNC
8�ł́C�ƒ댌���ɂ��Ă̌��y�͂���܂���D
����̍~���ڕW��10mmHg�オ�������Ƃ́C��N�i2013�N�j�ɕč����A�a�w��iADA�j�̐f�ÃK�C�h���C���̌����Ǘ��ڕW��10mmHg�オ��C130/80mmHg�ɂȂ������Ƃɒǐ�������̂ł��D����ɁC��������N�i2013�N�j�ɔ��s���ꂽ���B�������w��iESH�j�̐f�ÃK�C�h���C���ł��C80�Έȏ�ł͎��k��������150mmHg�����ɂ��邱�Ƃ𐄏�����Ă��邱�ƂƂ���v���܂��D���E�́C�~���ڕW���ɘa��������ɓ����Ă��܂��D
JNC 8 2014�i�č��j�������K�C�h���C�������Ǘ��A���S���Y��
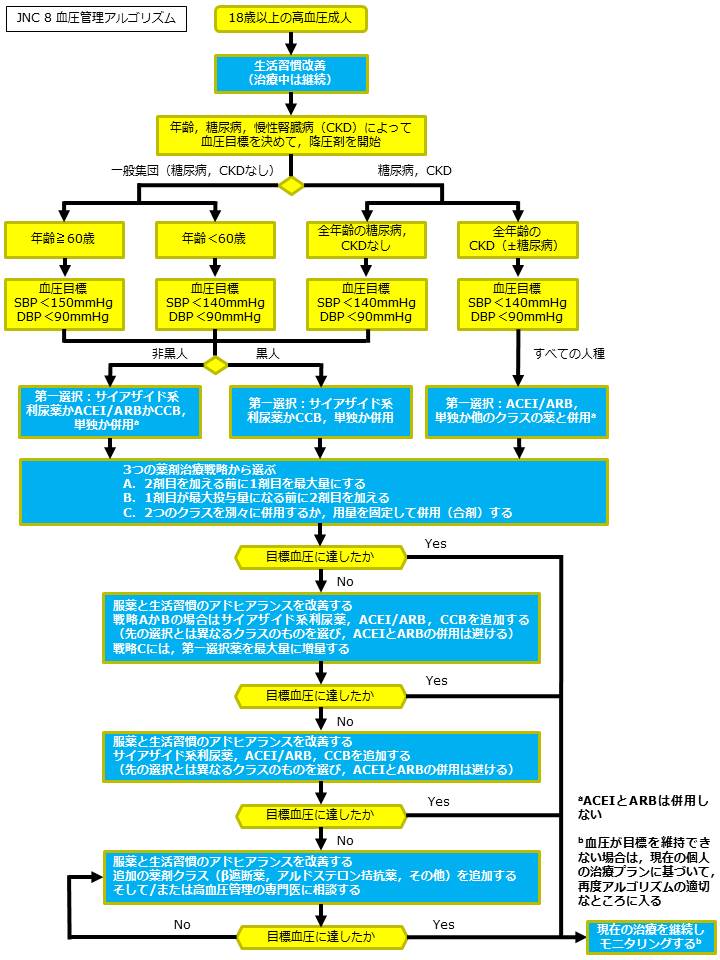
�i�I���W�i����Figure�j
JNC7����̕ύX�_
| �ύX�_ |
JNC 7 |
2014�������K�C�h���C���iJNC 8�j |
| ���@ |
�G�L�X�p�[�g�ψ���ɂ��C���܂��܂Ȍ����f�U�C�����܂ޑ̌n�I�ł͂Ȃ��������r���[
�R���Z���T�X�Ɋ�Â������� |
�G�L�X�p�[�g�p�l���ɂ���Ē�`����C���@�_�`�[���imethodology team�j�����͂������N���j�J���N�G�X�`�����ƃ��r���[�
���@�_�ҁimethodologist�j�ɂ����RCT�G�r�f���X�Ɍ��肳�ꂽ |
| ��` |
�m��f�f���ꂽ�������ǂƑO�������� |
�������ǂƑS�������ǂ̒�`�͎�����Ă��Ȃ����C���Â�臒l�͒�`���ꂽ |
| ���ẪS�[�� |
�u�P�����v�������Ƃ��܂��܂ȍ����ǁi���A�a��CKD�j�ɕ����Č��߂�ꂽ���ÃS�[�� |
���ʂ̏W�c�ł̈قȂ�S�[�����x������G�r�f���X���r���[������ꍇ�������āC�S���������҂ɑ��Č��߂�ꂽ�������ÃS�[�� |
| �����K���̐��� |
�������r���[�Ɛ��Ƃ̈ӌ��Ɋ�Â��������ꂽ�����K�����P |
Lifestyle Work Group���x������G�r�f���X�Ɋ�Â��������ɂ���Đ�������鐶�����P |
| ���� |
5�̃N���X�����I���̖�܂Ƃ��Đ������ꂽ���C��ނ����̃N���X��p����K�����Ȃ��w�ǂ̊��҂ł́C�T�C�A�U�C�h�n���A�܂����I���Ƃ��Đ��������
�Ⴆ�C���A�a�CCKD�C�S�s�S�C�S�؍[�ǁC�]�����C����CVD���X�N�̍����ǂ������҂ɓ�����������̍~���܃N���X
���O�ƒʏ�̓��^�ʂ͈̔͂��܂ތX���~���܂̕�I�ȕ\���܂� |
RCT�̃G�r�f���X�ɂ���Đ������ꂽ4�̖�܃N���X�iACEI�܂���ARB�CCCB�C���A�܁j����̑I���Ɠ��^��
�l��CCKD�C���A�a�T�u�O���[�v�ɑ���G�r�f���X���r���[�Ɋ�Â��Đ������ꂽ���ٓI�Ȗ�܃N���X
�p�l�����A�E�g�J�������ŗp�����Ă�����܂Ɠ��^�ʂ̕\���쐬���� |
| �g�s�b�N�͈̔� |
�������r���[�Ɛ��Ƃ̈ӌ��Ɋ�Â��ċL�q���ꂽ�����̖��i����������C���ҕ]���R���|�[�l���g�C���������C���W�����̃A�h�q�A�����X�C��R���������C����̏W�c�ł̍������j |
RCT�̃G�r�f���X���r���[�ɂ��C�p�l���ɂ���čł��d�v�Ɣ��f���ꂽ����I�Ȏ������舵���� |
| �o�őO�̃��r���[�v���Z�X |
39�l�̎�ȃv���t�F�b�V���i���C���I�C����юw�E�ȑg�D��7�l�̘A�M�E�����A�g����National High Blood Pressure Education
Program Coordinating Committee�ɂ���ă��r���[���ꂽ |
���Ƃƌ��I�g�D�C�A�M�E���ƘA�g�������Ƃɂ���ă��r���[���ꂽ�D������g�D����̃I�t�B�V�����ȃX�|���T�[�V�b�v�͂Ȃ� |
���̍������f�ÃK�C�h���C���̍~���ڕW�Ƃ̔�r
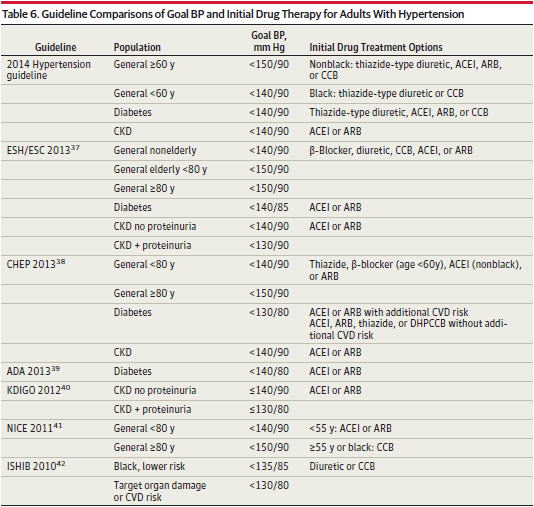
���̕\������ƁC���E�̍������f�ÃK�C�h���C�����~���ڕW���ȑO���Â����Ă���̂�������܂��D�p��NICE�̍������f�ÃK�C�h���C���iCG127�CNICE2011�j�Ȃǂ́C2011�N�̎��_�ŁC��ʐl�ł̍~���ڕW��140/90mmHg�����C80�Έȏ��150/90mmHg�����Ƃ��Ă��܂����D�����ESH/ESC�CADA�Ȃǂ����X�ƒǏ]����Ƃ����̂����E�I�ȗ���ł��邱�Ƃ�������܂��D
���{�ł́CJSH2014�ō~���ڕW�������グ���C�����������A�a��CKD���҂ł�130/80mmHg�����Ƃ��邱�Ƃɂ��Ă��܂����CJSH2014�쐬�ψ������{�a���搶�̃R�����g�i�L���v�`���j�ł́C�u�S�؍[�ǂ̑������Ăł́A���i�ȍ~���ɂ��S�؍[�ǃ��X�N�̗L�ӂȒቺ��������Ȃ��������Ƃ��d�����ꂽ�B�������A���{�ł͔]�������ǃ��X�N�ɂ����ڂ��ׂ��ŁAACOORD-BP�����ł��]�����͋����Ö@�Q�ŏ��Ȃ��A120mmHg�����܂ʼn�����Δ]�������X�N�͖�40%����Ƃ̌������ł���B���{�̎���ɍ������~���ڕW���\�z�������v�Ƃ̍l���������Ă��܂��D�������C���̍l�����́C���̂ǂ̐f�ÃK�C�h���C���ɂ�����܂���D2013�N��ADA��Position statement�ł��C�]�������Ǘ����Ⴂ���߂ɁC����p�����Ă���Ƃ��ϋɓI�ȍ~���͊��߂��Ȃ��Ƃ���܂��D���A�a���҂ɂ����錌���Ǘ��ɏڍׂ������܂������C����͓��{�ł������ł���C�����_�ŐϋɓI��130/80mmHg�����ɂ������������ƌ��_�t����͍̂���Ǝv���܂��D
JNC 8�i�č��j�쐬���@
�K�C�h���C���쐬�ψ�
JNC 7�ł͍������C�t���C�z��̐��Ƃ݂̂ō쐬����Ă��܂������CJNR 8�ł́C�������i14�l�j�C�v���C�}���E�P�A�i6�l�j�C�V�N�a�i2�l�j�C�z��i2�l�j�C�t���i3�l�j�C�Ō�i1�l�j�C��w�i2�l�j�C�Տ������i6�l�j�CEBM�i3�l�j�C�u�w�i1�l�j�C���w�i4�l�j�C�P�A�V�X�e���̒��Őf�ÃK�C�h���C���̊J���Ǝ��{���s���Ă���l�i4�l�j�́C�����l48�l�̐��Ƃ��I��ăp�l�������o�[�ɂȂ�܂����D�l�X�ȕ���ɓn���Đl���W�߂��̂͗ǂ����Ƃł����C�܂�����ł͕s�\���ł��D�f�ÃK�C�h���C�����쐬����ۂɂ́C�����闘�Q�W�҂��W�܂��ăK�C�h���C���p�l�������Ȃ��Ƃ����܂��CJNC
8�̐����쐬�ɂ́C���ҁC�s���C���n�r���ȂǑ厖�ȃX�e�[�N�z���_�[�������ݎQ�����Ă��܂���D�����C�]���̐f�ÃK�C�h���C���ł͂��܂茩���Ȃ����������鍂�����f�Â̐��ƈȊO�̃v���C�}���E�P�A��C�Ō�t�C��t�ȂǕ��L������̃G�L�X�p�[�g���W�߂�ꂽ�Ƃ����͉̂���I�ł��D
JNC 8�ł�COI���J������Ă��āC17�l��4�l�i24%�j�̈ψ�����Ƃ���Ӌ����Ă����Ƃ���܂��D���Ȃ݂ɂ���4�l�́CSuzanne Oparil, MD�CWilliam C. Cushman, MD�CRaymond R. Townsend,
MD�CJackson T. Wright Jr., MD, PhD�ŁC���ꂼ��S������C����������C�t������C����������ł��D
����ɁC�K�C�h���C������������2013�N1���ɁC�O���]���Ƃ��āC16�l�̐��Ɓi�z��C�t���C�v���C�}���E�P�A�C��w�C�Տ������C�������v�w�C���̑��̏d�v�Ȋ֘A�̈�j��5�l�̘A�M���{�@�E�����ւ���Ă��܂��D
Clinical questions
JNC 8�ł́C��I�ȍ������f�Â̐����������̂ł͂Ȃ��C�p�l�����I�ȉ��̗Տ���3�̋^��ɓ������Đf�ÃK�C�h���C���쐬���s���܂����D
1�D���������l�ɂ����āC����̌���臒l�o�~�����Â��J�n���邱�Ƃ́C���N�A�E�g�J�������P���邩�H
2�D���������l�ɂ����āC����̌����ڕW�ւ̍~���܂ɂ�鎡�ÂŁC���N�A�E�g�J���͉��P���邩�H
3�D���������l�ɂ����āC���܂��܂ȍ~���܂�~���܂̃N���X�́C����̌��N�A�E�g�J���ɑ��ė��v�ƊQ���قȂ邩�H
|
�G�r�f���X���r���[
JNC 8�́C���̍쐬��GRADE system��p���Ă��܂���D������肩�V�X�e�}�e�B�b�N���r���[�����Ă��܂���D�o�Ńo�C�A�X�̉\�����ӎ����Ȃ���Ȃ�܂���D
18�Έȏ�̐��l��ΏۂƂ����������̌����ɏœ_�Ă܂����D�ȉ��̗\�ߌ��߂�ꂽ�T�u�O���[�v�Ɋ֘A���錤�����W�߂Ă��܂��F���A�a�C�����������C�������������C�S�s�S�C�����]�����C�����t���a�iCKD�j�C�`���A�C����ҁC�j���Ə����C�l��C�i���ҁD�T���v���T�C�Y��100�ᖢ���̌����C1�N���������ǐՂ��Ă��Ȃ������͏��O���܂����D����͂��C�x���g���ǐ������Ȃ����߂ɐM�������Ⴍ�Ȃ��Ă��܂�������r������Ƃ����ړI�ł��i�������C�V�X�e�}�e�B�b�N���r���[�̊T�O�ɔ����܂��j�D����ɁC�A�E�g�J���Ƃ��āC�ȉ��̂��̂������������������̗p����Ă��܂��D
�@�E�����S�C�S���ǎ����iCVD�j�֘A���S�CCKD�֘A���S
�@�E�S�؍[�ǁC�S�s�S�C�S�s�S�ɂ����@�C�]����
�@�E���������ǍČ��p�i�������o�C�p�X�p�C�������`���p�C�������X�e���g�}���p�j�C���̑��̌��ǍČ��p�i���C�t�����C�����������ǍČ��p���܂ށj
�@�E�����t�����iESRD�j�i�Ⴆ�Γ��͂�t�ڐA���s���Ă���t�s�S�j�C�N���A�`�j�����x���̔{���C�������h�ߗ��iGFR�j�̔���
�p�l���͍ēǂ���G�r�f���X��RCT�Ɍ������܂����D���̍l����GRADE system�Ƌ��ʂ��Ă��܂��D
�ŏ��̌����́C1966�N1��1���`2009�N12��31����Ώۂɍs���C���̌�PubMed��CINAHL��p����2�l�̃p�l�������o�[2009�N12���`2013�N8���ɂ��Č������܂����D���̌��ʂ́C3�l�̃p�l�������o�[�����r���[���܂����D����2��ڂ̌����ŁC�p�l���͈ȉ��̑g�ݓ����ɐ������܂����D
�@1�j�������̃��W���[�Ȍ����������i�Ⴆ��ACCORD-BP�CSPS3�j
�@2�j�Q���҂�2,000�l�ȏ�������
�@3�j���{����������
�@4�j���̑��̑S�Ă̑g�ݓ���^���O��ɓ��Ă͂܂���
�I�ꂽ�����́CNHLBI�̕W�������]���c�[���istandardized quality rating tool�j��p���Ď����]������Cgood��fair�̏ꍇ�Ɍ���g�ݓ�����܂����D
�O���̕��@�_�`�[�����C�������r���[���s���C�I�ꂽ�_������f�[�^���G�r�f���X�e�[�u���ɂ܂Ƃ߁C�G�r�f���X�̂܂Ƃ߂����܂����D���̃G�r�f���X���r���[����C�p�l���̓G�r�f���X���������C�e�����ɂ��ē��ӂ��s���ӂ��𓊕[���܂����D���F���ꂽ�G�r�f���X�����ɂ��āC����Ƀp�l���̓G�r�f���X�̎��ɂ��ē��[���܂����iTable
2�j�D�S�Ă̏d��Ȏ���ɂ��ẴG�r�f���X���������܂�����C�p�l���͗Տ��I�Ȑ�������邽�߂ɃG�r�f���X���������r���[���C�������Ƃ��̋����ɂ��ē��[���܂����iTable
3�j�D�G�r�f���X�����Ɛ����̗����ɂ��āC���[�i���C�����j�̋L�^�́C���L���ōs���܂����D�p�l���͉\�Ȃ�100%�̃R���Z���T�X��ڎw���܂������C2/3�ȏ�̎^���ʼn��Ƃ��܂����D�������C���Ƃ̈ӌ��Ɋ�Â���������75%�����ӂ���ΔF�߂邱�Ƃɂ��܂����D
�}�C�m���e�B�[�̈ӌ�
JNC 8�ł́C�}�C�m���e�B�[�̈ӌ��Ƃ��āC�����ɔ��_����_�������\����Ă��܂��D
����1�̓��A�a��CKD�������Ă��Ȃ�60�Έȏ�̍���҂ł̍~���ڕW���C140/90mmHg��������150/90mmHg�����Ɉ����グ��ꂽ���Ƃɔ������K�C�h���C���p�l���̃}�C�m���e�B�[�̎咣���CAnn Intern Med�iAnn Intern Med. 2014;160(7):499�j�Ɍf�ڂ��ꂽ�D150/90mmHg�����ɂ���̂��x�����閾�m�ȃG�r�f���X���Ȃ����炾�Ƃ��Ă���D�����}�C�m���e�B�[�������l�����́C����������C�t������C�z������������D
���m�ȃG�r�f���X���Ȃ�������ϋɓI�Ɏ��Â���̂��C�G�r�f���X���Ȃ������莡�Âɂ͕ێ�I�ɂȂ�̂��C�X�^���X�̈Ⴂ�Ƃ�������D�}�C�m���e�B�[�̈ӌ�����������Č��J����邱�Ƃ́C�����ɂȂ肪���ȃK�C�h���C���p�l����c�̓��������m�ۂ��邽�߂ɂ��d�v�ł���D
�����C�}�C�m���e�B�[��80�Έȏ�ł�150/90mmHg�����ɂ��邱�Ƃɂ͓������Ă���C����́C���BESH/ESC�K�C�h���C���C�J�i�_CHEP�K�C�h���C���C�č�ACC/AHA�K�C�h���C���C�p��NICE�K�C�h���C���C�č�ASH/ISH�K�C�h���C���Ƃ����ʂ���Ƃ̎咣���D
�Ȃ��CAnn Intern Med�Ɍf�ڂ��ꂽ�_���̕M�����҂�Jackson T. Wright Jr., MD, PhD������������ł���C�K�C�h���C���p�l��17�l����Ƃ���Ӌ����Ă���4�l��1�l�ł��邱�Ƃ��CCOI�J���Ŏ�����Ă��邱�Ƃɂ����ӁD
JNC 8�i�č��j�ɂ�����G�r�f���X�̎��Ɛ����̋���
JNC 8�ɂ�����G�r�f���X�̎��̕��ފ�iGRADE system�Ƃ̓G�r�f���X�̎��̕]������قȂ�̂Œ��Ӂj
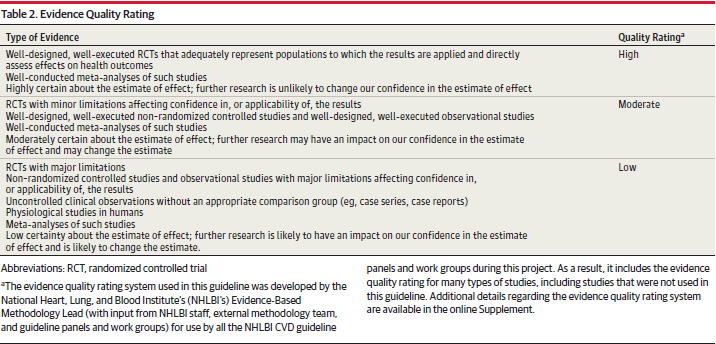
JNC 8�ɂ����鐄���̋����iGRADE system�ɂ�鐄���̋����Ƃ͈Ⴄ�̂Œ��Ӂj

JNC 8�̌��E
JNC 8�ɂ͂������̌��E������܂��D�{�����Ŏw�E����Ă���̂́C�ȉ��̓_�ł��D
�܂��C��I�Ȑf�ÃK�C�h���C���ɂȂ��Ă��炸�C3��Cliical Question�Ɍ��肵�Đ��������t�����Ă��܂��D
����ɁC�G�r�f���X���r���[�ɂ́C�ώ@�����C�V�X�e�}�e�B�b�N���r���[�C���^�A�i���V�X���܂܂�Ă��܂��C�p�l�������^�A�i���V�X�����Ă���킯�ł�����܂���D
JNC 8�ł́C����������Ȋ��҂̌����͔r������Ă���̂ŁC����������Ȋ��҂ɂ́C�����̐����Ă͂߂邱�Ƃ͂ł��܂���D
�ӎ�
JNC 8�̓��e����ɂ������ẮCMD Anderson Cancer Center�̍��X�؍G���搶�ɖ��Ȃǂ̃`�F�b�N�����Ă��������܂����D���̏����Ċ��ӂ������܂��D
�@��������̕��@
 �����̑�����@�i���ڐV�݁C2014/2/20�C�ŏI�X�V2014/2/20�j �����̑�����@�i���ڐV�݁C2014/2/20�C�ŏI�X�V2014/2/20�j
���{�������w��̍��������ÃK�C�h���C���iJSH�j2014�i�āj�ł́C�u1��2�ӂ̑���ŁC1�@��Ɍ���2��̑���Ƃ��C���ϒl�����̋@��̌����l�Ƃ��ėp����v�Ƃ����悤�ɒ�߂Ă��܂��D
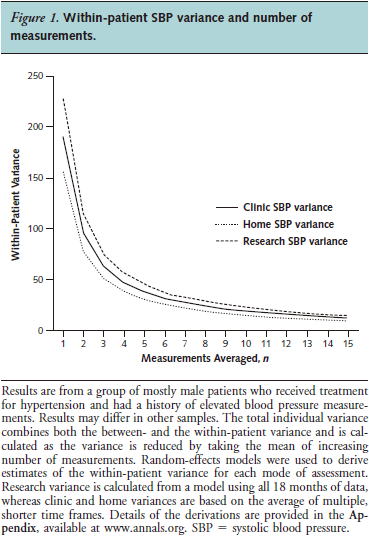
1�@��̌����̑���ɂ��ẮC����1��ڂ̌����l�Ƃ���ȍ~�̒l�̗������傫���C�𑝂₷���ɕ��ϒl�̕ϓ����������Ȃ�C�قƂ�Ǖς��Ȃ��Ȃ�܂łɂ�4�`6��ȏ�̑��肪�K�v�Ƃ����������ʁiAnn Intern Med 2011;154:781�j������܂��DFigure 1�ł́CResearch SBP variance�i�����{�݂ő��肵�����k�������ϓ��j�CClinic SBP variance�i�f�@���ő��肵�����k�������ϓ��j�CHome
SB variance�i����ő��肵�����k�������ϓ��j�̏��ɕϓ����������Ȃ邱�Ƃ�������܂��D
���̘_���ł͌��_�Ƃ���5��ȏ㑪�肵�����ϒl�𑪒肷��悤�ɐ������Ă��܂����C�������Ɍ����I�ł͂���܂��C�^�ʖڂŐ_�o���ȌX���ɂ�����{�l�́C�������đ��肷�邲�Ƃɕs���ɂȂ��Č����̒l���㏸���Ă��܂���������܂���D
�l�I�ɂ�1�@��̌�������́C3����x�s���̂��悢�Ǝv���Ă��܂��D�܂����ϒl�ł͂Ȃ��āC�Ⴂ���̒l���̗p���ċL�^���Ă�����Ă��܂��D�����1��ڂ̑���l�������������������Ȃ��Ă��܂����Ƃ��������߁C���ϒl�ł�1��ڂ̒l�Ɉ��������č��߂ɏo�Ă��܂������ꂪ���邩��ł��D�����l�͌������㍂���l���o�邱�Ƃ͑����Ă��C�Ⴂ�l���o�邱�Ƃ͂���قǑ����Ȃ���ۂł��D���҂ɂ���Ă�1��ڂ̌����l������ȍ~�Ƃ��قǕς��Ȃ��ł����C���̂悤�ȏꍇ��1�@��1�肾���ł��ǂ��ł��傤�D���Ɣӂ̌����l�ɂ��܂�Ⴂ���Ȃ��ꍇ�ɂ́C��1��̑��肾���ł��ǂ��Ǝv���܂��D
��������̕��@�̂܂Ƃ�
| ���� |
���e |
| ����� |
�Â��œK���Ȏ�����
�֎q�ɍ����ă����b�N�X����
����g�܂��ɁC�b�������� |
| ������� |
�N����1���Ԉȓ���
�r�A���
������܂���
���H�O��
1�`2�����Âɂ��� |
| ����� |
1��2��i��1��ł��j
1�@��̑����2�`3��i�ϓ������Ȃ��ꍇ��1��ł��j
���肵�Ă���C��������łȂ��Ă��ǂ�
�s����̏ꍇ�́C�������肷�� |
| �]�� |
�����肵���ꍇ�͈�ԒႢ�l�i�K�C�h���C���ł͕��ϒl�j
�������F135/85mmHg�ȏ�
���퍂�l�����F125/80mmHg�`135/85mmHg
���파���F125/80mmHg���� |
�@�{�Ԑ���������
 �~���ڕW�@�i���ڐV��2018/1/13�j �~���ڕW�@�i���ڐV��2018/1/13�j
�{�M�̍��������ÃK�C�h���C��2014�iJSH2014�j�C�p��NICE�̍������f�ÃK�C�h���C���iCG127�CNICE2011�j�C�č���JNC8�i�č������������ψ����8���j�̐����ł́C���������̂Ȃ����҂̍~���ڕW��140/90 mmHg�����ƂȂ��Ă��܂��D�ȉ��ɁC�G�r�f���X��������܂��D
2015�N�ɍ~���ڕW�����k������140 mmHg�����ɂ���̂�120 mmHg�����ɂ���̂Ƃ��r����50�Έȏ�̍��������҂�ΏۂƂ���SPRINT�����iN Engl J Med 2015;373:2103�j�̌��ʂ����\����C120 mmHg�����ɂ����ق����S���ǃC�x���g���L�ӂɌ���Ƃ����̂ő傫�Șb��ɂȂ�܂����D�������C���̎�v�A�E�g�J���͕����A�E�g�J���ł���C�ʂ̃A�E�g�J���ł́C�S�؍[�ǁC�}�����nj�Q�C�]���������炳���C�S�s�S�͔N��0.67 %����0.41 %�ցC�S���ǎ��͔N��0.43 %����0.25 %�ցC�����S�͔N��1.40 %����1.03 %���炵�C�t�@�\�����͔N��0.35 %����1.21 %�ɑ�����Ƃ������̂ł����D����̃A�E�g�J���ŗL�Ӎ��͂��܂������C���̂قƂ�ǂŗՏ��I�ɂ͌��ʂ������ł��Ȃ����炢���������̂ł����D
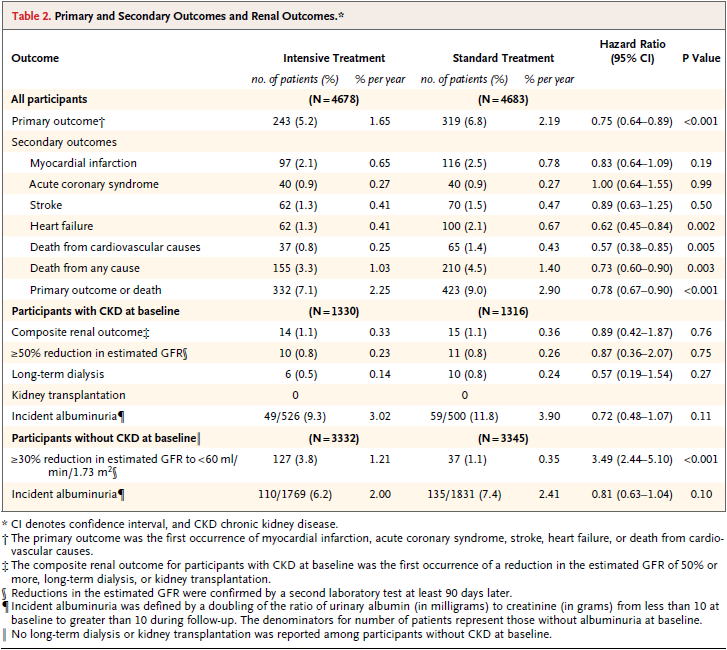
����́C75�Έȏ�̃T�u�O���[�v��́iJAMA 2016;315:2673�j�ł��C���l�̌��ʂł����D���������āC���̌����̌��ʂ𗝗R�ɁC�����Ǘ������k��������140 mmHg�������������邱�Ƃɂ͓��ݐ�܂���D
2009�N�ɍ~���ڕW����������7����RCT�̃R�N�������r���[�iCDSR 2009:CD004349�j�̌��ʂ����\����܂������C�ڕW�l������135/85 mmHg������140�`160/90�`100 mmHg�����̊ԂɈႢ�͂���܂���ł����D
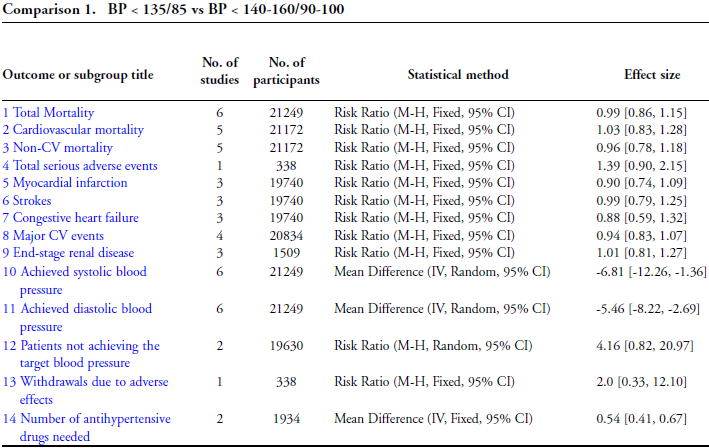
2016�N�ɂ�19����RCT�̃V�X�e�}�e�B�b�N���r���[�iLancet 2016;387:435�j�̌��ʂ����\����C����������ό�����133/76 mmHg��140/81 mmHg�̔�r�ŁC��͂��v�ȐS���ǃC�x���g�Ɣ]�����C�A���u�~���A�͂��ꂼ��RR 0.86�i0.78�`0.96�j�{��0.78�i0.68�`0.90�j�{�C0.90�i0.84�`0.97�j�{�ɗL�ӂɌ���܂������C����ȊO�̃A�E�g�J���ɂ��Ă͕ς��͂���܂���ł����D
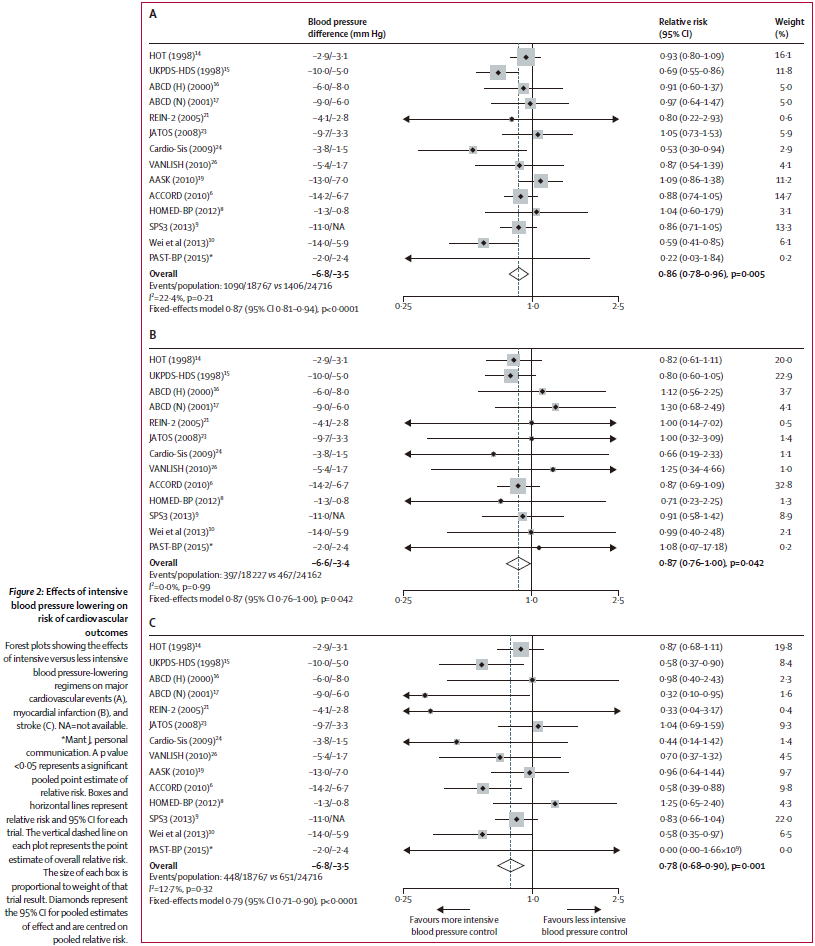
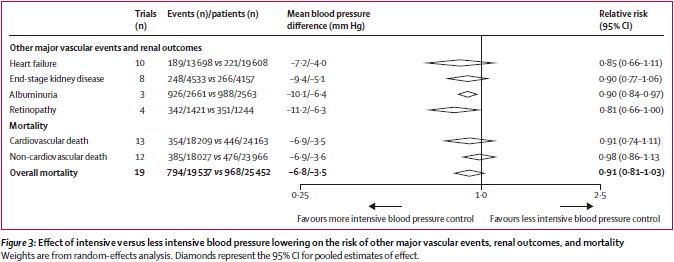
�ȏォ��C���������̂Ȃ����҂̍~���ڕW��140/90 mmHg�����ŗǂ��ƍl�����܂��D
�������҂ł́C2017�N��3����RCT�̃R�N�������r���[�iCDSR 2017:CD011575�j�̌��ʂ����\����Ă���C�~���ڕW150-160/95-105 mmHg������140/90 mmHg�����ł͑����S�C�]�����C�S���ǃC�x���g�C�L�Q���ۂɂ�钆�f�̑S�ĂňႢ�������܂���ł����D���̌��ʂ���C����҂ł�150/90 mmHg�������~���ڕW�Ƃ���Ηǂ��Ƃ����܂��D
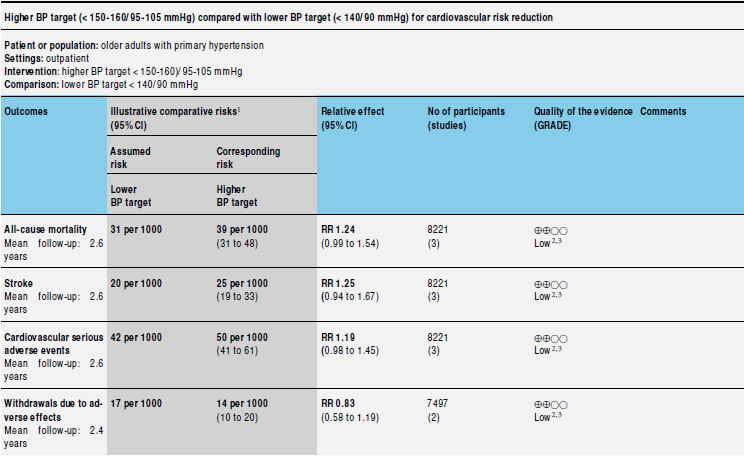

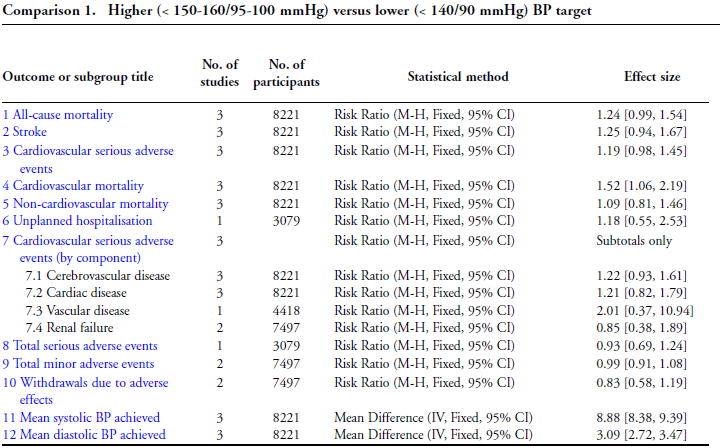
 �~���܂̑I�ѕ��@�i���ڐV��2014/1/14�C�ŏI�X�V2018/1/13�j �~���܂̑I�ѕ��@�i���ڐV��2014/1/14�C�ŏI�X�V2018/1/13�j
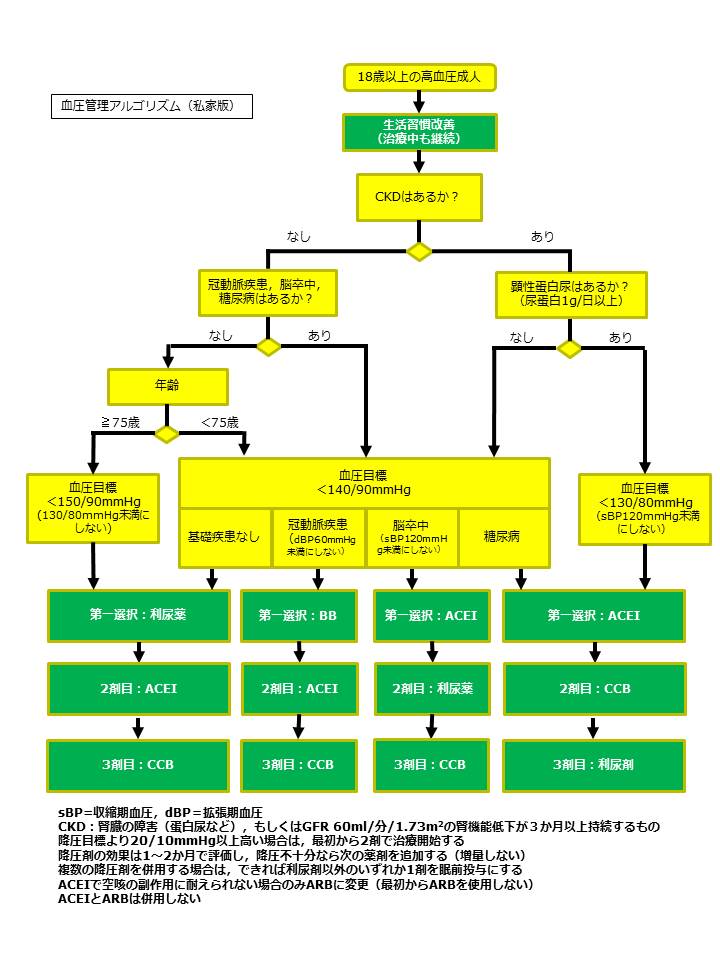
�{�M�̍��������ÃK�C�h���C��2009�iJSH2009�j�C�p��NICE�̍������f�ÃK�C�h���C���iCG127�CNICE2011�j�C�č���JNC8�i�č������������ψ����8���j���Q�l�ɁC�Ǘ��҂��l�����~���܂̑I�ѕ��̃A���S���Y�����ȉ��Ɏ����܂��D
�{�M�̐f�ÃK�C�h���C���́C���������ÃK�C�h���C��2014�iJSH2014�j��update����Ă��܂����C�ȉ��̃A���S���Y���ɕύX�͂���܂���D�ނ���C����܂Ō����������~���ڕW���C�O�̂��̂Ɛ����������悤�ɂȂ�܂����D
 �~�����A��͂ǂ��I�Ԃ��@�i���ڐV��2016/2/12�C�ŏI�X�V2018/1/15�j �~�����A��͂ǂ��I�Ԃ��@�i���ڐV��2016/2/12�C�ŏI�X�V2018/1/15�j
�~�����A��̎��
�~�����A��̓`�A�W�h�n���A��ƃ`�A�W�h�n�ގ���ɕ�����܂��D
|
��ʖ� |
���i�� |
�K�i |
�Y�t�����L�ڗp�� |
�����p�� |
�� |
| �`�A�W�h�n���A�� |
�q�h���N�����`�A�W�hHCTZ |
�攭�i�̔����~�C�㔭�i���� |
12.5 mg/25 mg |
25�`100 mg |
12.5�`25 mg |
5.6�~�^5.6�~ |
| �@�g���N�������`�A�W�h |
�t���C�g����(R) |
1 mg/2 mg |
2�`8 mg |
1�`2 mg |
9.6�~�^9.6�~ |
| �`�A�W�h�n�ގ��� |
�C���_�p�~�h |
�i�g���b�N�X(R) |
1 mg/2 mg |
2 mg |
1�`2 mg |
11.4�~�^21.5�~ |
| �N�����^���h��CTD |
�n�C�O���g��(R)�C�����̔����~ |
25 mg |
25 mg |
25 mg |
|
�`�A�W�h�n�ގ���̂ق����C�`�A�W�h�n���A�������~�����ʂ��傫���Ƃ���C2014�N�̃R�N�������r���[�iCochrane Database Syst Rev. 2014 May 29;5:CD003824�j�̌��ʂł́C�ȉ��̂悤�ɂȂ��Ă��܂��D
|
��ʖ� |
�K�i |
�~������ |
| �`�A�W�h�n���A�� |
�q�h���N�����`�A�W�hHCTZ |
12.5mg |
-6.27mg�i-7.24�`-5.31�j |
| �`�A�W�h�n�ގ��� |
�C���_�p�~�h |
1mg |
-8.69mg�i-9.96�`-7.42�j |
| �N�����^���h��CTD |
25mg |
-13.64mg�i-16.03�`-11.25�j |
�Ȃ��C�~�����ʂɗp�ʈˑ����͌����܂���D
2015�N�̃V�X�e�}�e�B�b�N���r���[�iHypertension 2015;65:1041�j�ł��C�C���_�p�~�h�̂ق����q�h���N�����`�A�W�h�������k��������5.13 mmHg�Ⴉ�����Ƃ������ʂł����D
�`�A�W�h�n���A�܂ƃ`�A�W�h�n�ގ���̂ǂ����I�Ԃׂ����H
���E�ő�K�͂̍������������Ì����ł���ALLHAT�����ł͗��A��ɂ̓N�����^���h�����g�p����܂������C�N�����^���h����HCTZ��1.5�`2�{���ʂ���������Ƃ���Ă��܂��D�����āCHCTZ�͐S���ǃC�x���g��\�h���邱�Ƃ�RCT�ŏؖ��ł��Ă��܂���D������������C�~�����ʂ��ア���Ƃ��W���Ă��邩������܂���D
�ł�����C�{���̓`�A�W�h�n�ގ���ł���N�����^���h�����g�p�������̂ł����C�����ł͔̔����~�ɂȂ��Ă��܂��܂����̂ŁC����ɓ����`�A�W�h�n�ގ���ł���C���_�p�~�h���g�������ƍl����͎̂��R�ł��D
�~���ڕW�̒B�����l�����ꍇ�ɂ̓i�g���b�N�X1mg���������邱�Ƃ̓��[�Y�i�u���������ꂸ�C�����ɂ�������Ă����t������悤�ł����C�����l�I�ɂ͌덷�͈͂��Ǝv���̂łǂ���ł������Ǝv���܂��D���@�ł͉@���̗p��ł���t���C�g����(R)1mg���g�p���Ă��܂��D
���ۂɁC�R�z�[�g�����ł͂���܂����C�N�����^���h����HCTZ�͐S���ǎ��S�Ɠ��@�������ł���Ƃ������ʂ��o�Ă��܂��iAnn Intern Med 2013 Mar 19;158(6):447�j�D�����āC���̂ق����������ł��D
��ʓI��JNC8�ɂ�������Ă���悤�ɁC�~���܂͗Տ������ŗp����ꂽ�p�ʂ��g�p���邱�Ƃ����ʂ邽�߂ɏd�v�ł��D���A��ȊO�̍~����͍����̓Y�t�����p�ʂ̍ő�e�ʂ܂ő��ʂ���ׂ��ł����C���A�܂͗p�ʈˑ����ł͂Ȃ����ʂɂ�蕛��p�������邨���ꂪ����̂ŁC���ʂŎg�p���܂��D�t���C�g����(R) 1�`2mg�܂ŁCHCTZ 12.5�`25mg�܂ŁC�i�g���b�N�X(R)
1�`2mg�܂łł��D
 ARB����I���ɂ��Ȃ����R�@�i���ڐV��2014/3/6�C�ŏI�X�V2018/1/13�j ARB����I���ɂ��Ȃ����R�@�i���ڐV��2014/3/6�C�ŏI�X�V2018/1/13�j
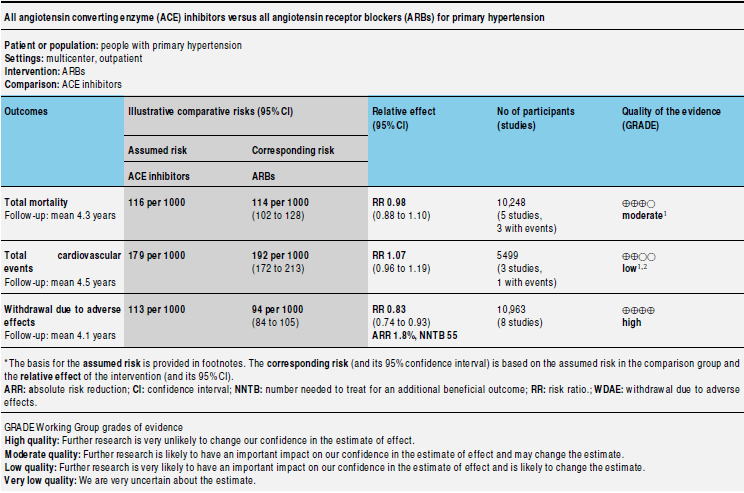
ACE�j�Q���ARB�̃G�r�f���X
ACE�j�Q���ARB�̌��ʂ��r�����R�N�������r���[�iCDSR 2014:CD009096�j��2014�N�ɔ��\����Ă���C�����ł́C�����S�ƐS���ǃC�x���g�ɂ͍��͂Ȃ��C�L�Q���ۂɂ��E����ARB�̕��ŏ��Ȃ��Ƃ������ʂł����D

ARB�̔F�e���͏d������ׂ���
�uARB��ACE�j�Q������F�e���������̂�ARB����I���Ƃ��ׂ��v�Ƃ����b���悭�����܂��D�������C���̎��́u�F�e���v�Ƃ́CACE�j�Q��̕���p�ł����P��ARB�ł͏��Ȃ����Ƃ��w���Ă���悤�ł��D
�������CACE�j�Q��̋�P�͒j����1���C������3�����x�ɂ����N���炸�C�ʏ�͎��ÊJ�n1�`2�T�ȓ��ɔ������܂��D�������C�t�I�Ȃ��̂ł���C�ʏ�����Ò��~����4�`7���ȓ��Ɏ���܂��iAnn Intern Med 1992;117:234�j�D
���̂��߁C�܂���ACE�j�Q��������Ĉ������Ƃ͂���܂���D���Ƃ��ƋN����Ȃ��l�̂ق��������킯�ł�����C�������čŏ�����ARB�ɂ���Ƃ����̂͗��\�Șb�ł��D
�x���\�h����
2004�N�CACE�j�Q��ɂ͔x���\�h���ʂ����邱�Ƃ����k��w�̌����iAm J Respir Crit Care Med 2004;169:1041�j�Ŏ�����b��ɂȂ�܂����D�S�̂Ƃ��Ă͗L�Ӎ��͂��܂���ł������C�A�W�A�l�ł�ACE�j�Q��͔x���̃��X�N��47�i14�`67�j%�L�ӂɌ��炷�Ƃ������ʂł����D��A�W�A�l�ł́C�L�ӂȍ��͔F�߂��܂���ł����D
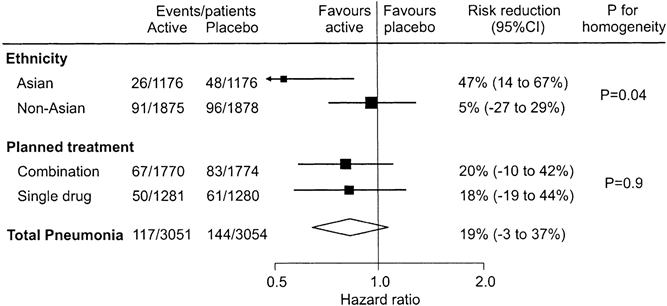
2012�N�CACE�j�Q���ARB�̔x���\�h���ʂ��������V�X�e�}�e�B�b�N���r���[�iBMJ 2012;345:e4260�j�����\����CACEI�͔x�����I�b�Y��0.66�i95%�M�����0.55�`0.80�j�Ɍ��炵�܂������CARB�ɂ͗L�ӂȍ����݂��܂���ł����D���̂悤�ɁCACEI��ARB�ɂ͂Ȃ��t�����l������܂��D
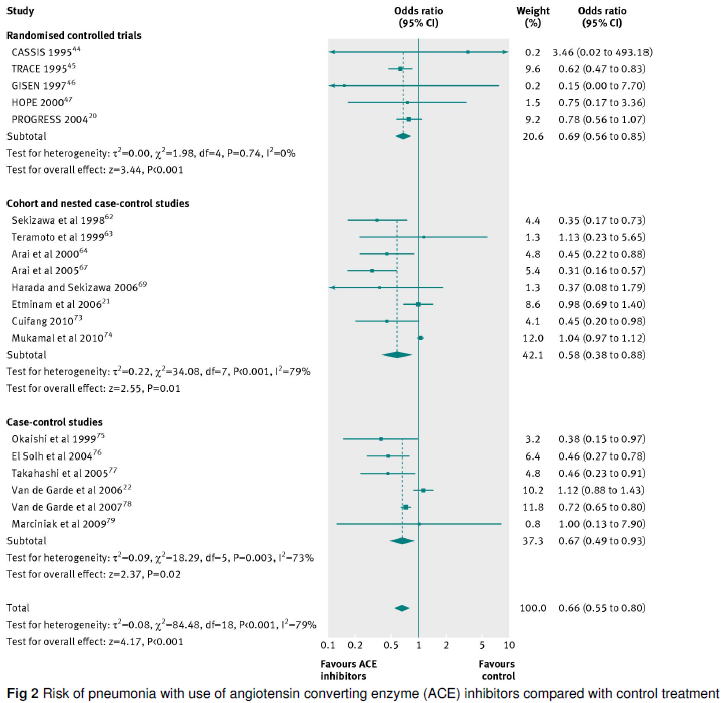
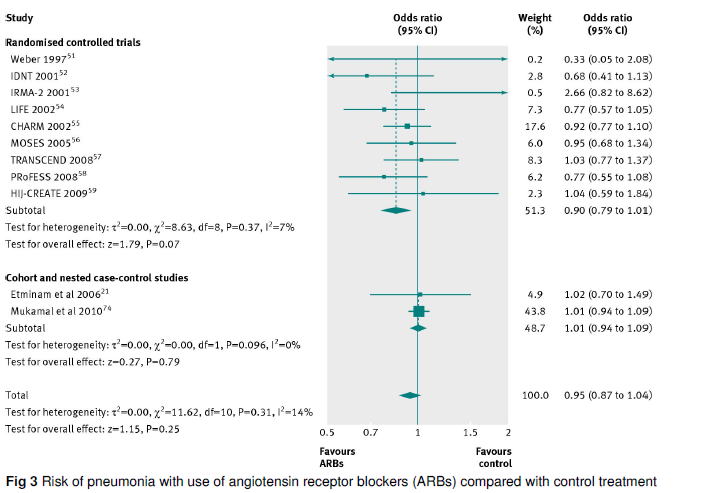
ARB��ACE�j�Q��ɗD�悳����ׂ��ł͂Ȃ�
�ȏ�܂��āC���W���A���M�I�e���V���j�Q����g�p����ۂɂ́C
�@1�jACE�j�Q���ARB�͌��ʂ�����
�@2�jACE�j�Q��̕���p�ł����P��1�`3�����x�ɂ����N�����C�������t�I�Ȃ̂ŁCARB�̔F�e����D�悳����ׂ��ł͂Ȃ�
�@3�jACE�j�Q��ɂ�ARB�ɂ͂Ȃ��x���\�h���ʂƂ����t�����l������
�@4�jARB�̂ق���������
�Ƃ��������R����C���ACE�j�Q����g�p���C�����P�̕���p���o�����C��Ԃ��̂��߂ɐQ���Ȃ��ȂǓ��퐶���Ɏx����������Ă���悤�Ȃ�CARB�ɕύX�����C�Ƃ����g����������ׂ��ł��傤�D
ARB���W�F�l���b�N���i�����ւ��ꂽ�̂�ACE�j�Q��Ƃ̖��͂����ԏk�܂��Ă��܂������C2018�N1�����݂ŁCACE�j�Q��ł���^�i�g���� �ƃC�~�_�v���� 5mg�̖�54.4�~�C30.3�~�������̂ɑ��āCARB�ł���f�B�I�o���ƃo���T���^��80 mg�̖�99.6�~��39.6�~�Ƃ�͂荂���ł��D
�]�����}�����̌����Ǘ��@�i���ڐV��2010/1/14�C�ŏI�X�V2014/10/30�j
�]�����}�����̌����Ǘ��ɂ��ẮC�]�������ÃK�C�h���C��2009�ł̐���
�]�����}�����̌����Ǘ�
�m�����n
1�D�]�������ǒ���̍������ɑ���Ǘ��́C���������\�ǁC���������o���������^����ꍇ�ȊO�͕a�^�f�f���m�肵�Ă���s���ėǂ��D�܂��~������g�p����O�ɁC�ɂ݁C�q�C�C�N���̏[���Ȃǂɂ�茌�����㏸���Ă���̂ł͂Ȃ������������ׂ��ł���D����C�������ጌ���i�V���b�N�j�͗A�t�C�Lj���Ȃǂő��₩�ɐ������ׂ��ł���i�O���[�hC1�j
2�D�]�[�Nj}�����ł́C���k��������220mmHg�܂��͊g����������120mmHg�̍���������������ꍇ��C�哮���𗣁E�}���S�؍[�ǁE�S�s�S�E�t�s�S�Ȃǂ��������Ă���ꍇ�Ɍ���C�T�d�ȍ~���Ö@�����������i�O���[�hC1�j
3�D����n��Ö@��\�肷�銳�҂ł́C���k��������185mmHg�܂��͊g����������110mmHg�ȏ�̏ꍇ�ɁC�Ö����^�ɂ��~���Ö@�����������i�O���[�hB�j�D |
�ȏ�̂悤�ɁC���}�����̌����Ǘ��ɂ��ẮC�����Ƃ��Ď��k��������220mmHg�̏ꍇ�Ɍ���~��������悤�ɐ�������Ă��܂��D
����C�������̌����Ǘ��ɂ��ẮC�ȉ��̂悤�ɐ�������Ă��܂��D
�]�[�ǖ������̌����Ǘ�
�m�����n
�]�[�ǂ̍Ĕ��\�h�ł́C�~���Ö@�����������D�ڕW�Ƃ��錌�����x���͏��Ȃ��Ƃ�140/90mmHg�����Ƃ���i�O���[�hA�j�D |
�������C�����ׂ����Ƃɖ������̒�`��������Ă��炸�C����������Ƃ��čl����悢�̂��s���ł���D
�]�����}�����̌����Ǘ��ɂ��ẮC���������ÃK�C�h���C��2009�ł̐���
���������ÃK�C�h���C��2009�ł́C�]�������}�����̌����Ǘ��ɂ��Ă̐����́C�h�\6-1�D�]���Ǐ�Q���������鍂�����̎��Áh�ɂ���C�ȉ��̂悤�ɂȂ��Ă��܂��D
|
�~�����ÑΏ� |
�~���ڕW |
�~���� |
���}����
�i����3���Ԉȓ��j |
����n��Ö@�\�芳��
SBP��185mmHg�܂��́C
DBP��110mmHg |
����n��Ö@�\�芳��
��185/110mmHg
����n��Ö@�J�n��
�i���Ȃ��Ƃ�24���ԁj
��180/105mmHg |
�j�J���W�s���C�W���`�A�[��
�j�g���O���Z������j�g���v���V�h�̔��ʓ_�H�Ò� |
�}����
�i����1-2�T�Ԉȓ��j |
�]�[�� |
SBP��220mmHg�܂��́C
DBP��120mmHg |
�O�l��85-90% |
�j�J���W�s���C�W���`�A�[��
�j�g���O���Z������j�g���v���V�h�̔��ʓ_�H�Ò�*1*2 |
| �]�o�� |
SBP��180mmHg�܂��́C
MBP��130mmHg |
�O�l��80% |
| �������i����1�����ȍ~�j*3 |
|
��140/90mmHg
�i���ÊJ�n1-3�����j*4 |
Ca�h�R��CACE�j�Q��C
ARB�C���A�܂Ȃ�*5 |
*1�@���W�������㏸������댯�ɒ��ӁD
*2�@�j�t�F�W�s���̐㉺���^�͋}���Ȍ����ቺ�������N�����댯������̂ŗp���Ȃ��D
*3�@�}�������Â��I������1-2�T�ォ��J�n���邱�Ƃ�����D
*4�@�����z�������x����C�]�劲�����ǂ̏ꍇ�͓��ɉ��������ɒ��ӁD���N�i�[�ǂ�]�o���ł́C140/90mmHg��肳��ɒႢ�~���ڕW�Ƃ���D
*5�@���A�a��S�[�ד��������҂ł�ARB�CACE�j�Q���p����D
�]�����}�����̌����Ǘ��ɂ��ẮCAHA/ASA�i�č��S���w��^�č��]�����w��j�ł̐���
AHA/ASA�FGuidelines for the Early Management of Adults With Ischemic Stroke�iStroke 2007;38:1655�j�F2007�N4���łɂ́C�}�������Âɂ����錌���Ǘ��ɂ��ẮC�ȉ��̂悤�ɐ�������Ă��܂��D
Class�T Recommendation�i�����j
5�D�������̃}�l�[�W�����g�ɂ��ẮC�Ȃ��c�_���c��D���Â̐������f�[�^�̓o���o���ł���C���_�Â����Ȃ��D�����̊��҂ł́C�]�������ǂ̍ŏ���24���ԂŎ��R�Ɍ�����������D���m���ȃf�[�^�������炳���܂ŁC���������Âɂ͐T�d�ȃA�v���[�`�����ׂ����Ƃ����������Ƃ����͈̂�ʓI�ɓ��ӂł���iClass�T�CLevel
of Evidence C�j�D�ϋɓI�Ȍ������Â��K�v�ȑ��̈�w�I�K�������銳�҂ł́C���Â��ׂ��ł���D���̐����͈ȑO�̃K�C�h���C������ς���Ă��Ȃ��D
8�D�������������㏸���Ă��銳�҂ō~�����邱�Ƃ͈�ʓI�ɓ��ӂ���邾�낤�D�����I�ȃS�[���͔]�������nj�n�߂�24���Ԃ�15%�܂ł̍~���ł���D�ǂꂭ�炢�ō~�����ׂ����͂悭�������Ă��Ȃ����C���k��������220mmHg�܂��͊g����������120mmHg�o�Ȃ�����C�Ö@�͍����T����ׂ��ł���Ƃ����R���Z���T�X������iClass�T�CLevel of Evidence C�j�D���̐����͑O��̃K�C�h���C������ς���Ă���C�~���̃S�[���ɂ��ĐV����������ꂽ�D�]������̍������̑������Â̌��ʂ������錤�������ݍs���Ă���D�p�l���́C���̊Ǘ����f���͂����肳���邽�߂̂�����f�[�^��҂��Ă���D
Class�U Recommendations�i�����j
1�D�}���������]�����ō~����̑I�ѕ��𐄏����邾���̃f�[�^���Ȃ��iClass�Ua�CLevel�@of Evidence C�j�DTable 10�ɂ��鐄���͈ȑO�̃K�C�h���C������ς�����D
2�D1���̗Տ������̃G�r�f���X�ł́C�]��������24���Ԉȓ��̍~�����͔�r�I���S�Ƃ��Ă���D���������āC���Ƃ��ƍ�����������C�_�o�w�I�Ɉ��肵�Ă����āC�~���܂��ĊJ���邱�Ƃɓ��ʂȋ֊����Ȃ����҂ł́C24���Ԉȓ��ɍ~������ĊJ���邱�Ƃ́C��ʓI�ɓ��ӂ����iClass�Ua�CLevel
of Evidence B�j�D
|
�{�M�̃K�C�h���C���ƈႢ�C�_�o�w�I�Ɉ��肵�Ă���C���@�O�ɍs���Ă����~���Ö@�̖�܂��C�]�������nj�24���Ԉȓ��Ɏn�߂ėǂ��Ƃ͂�����L�ڂ���Ă��܂��D
�����C���́C�u�_�o�w�I�Ɉ��肵�Ă���v�Ƃ����̂��ǂ�������Ԃ��w���̂��Ƃ������Ƃł��D
��ʓI�ɂ́C���ɃA�e���[�����]�[�ǂł͊K�i��̕a��̐i�s�𗈂����Ƃ����邽�߁C���ǂ���2�`3���o�߂��ώ@���Ȃ��ƕa���肵�Ă��邩�ǂ���������܂���D
�Ƃ������Ƃ́C������C���nj�24���Ԉȓ��ɍ~���܂��ĊJ����Ƃ����͕̂s�\�ɋ߂��̂ł͂Ȃ����Ǝv����킯�ł��D
�]�����}�����̌����Ǘ��ɂ��ẮCESO�i���B�]�����@�\�j�ł̐���
ESO�FGuidelines for Management of Ischaemic Stroke and Transient Ischaemic
Attack 2008�iCerebrovasc Dis 2008;25:457�j�F2008�N5���łɂ́C�}�������Âɂ����錌���Ǘ��ɂ��ẮC�ȉ��̂悤�ɐ�������Ă��܂��D
��ʓI�Ȕ]��������
Recommendations�i�����j
�E���[�`���ōs���~���͋}���]�[�ǂł͐�������Ȃ��iClass�W�CGCP�j
�E�J��Ԃ����肵�Ă��������ɂ߂č����i��220/120mmHg�j�ꍇ��C�d�ǐS�s�S�C�哮���𗣁C���������]�ǂ��������Ă���ꍇ�ɂ͒��Ӑ[���~�����邱�Ƃ����������iClass�W�CGCP�j
�E�}���ȍ~���͔����邱�Ƃ���������Ă���iClass�U�CLevel C�j
|
���̉���̖{�����ɂ́C�ȉ��̂悤�ɋL�ڂ���Ă��܂��D
�����Ǘ��i�����j
�]�����Ǘ��ɂ����錌�����j�^�����O�Ǝ��Â͋c�_�̕������̈�ł���D�]�[�nj�ŏ���24���Ԃ̌������ł������܂��͒Ⴂ���҂ł́C�����ɐ_�o�w�I�Ɉ������C�\�オ����[367]�D�i�����j����̐i�s���̌����ł́C�}���]������Ɍ�����������ׂ����C�����Ĕ]������̍ŏ��̐����ԁC�~���Ö@�𑱂���ׂ������~���ׂ������������Ă���[371�C372]�D
|
371: COSSACS investigators: COSSACS (Continue or Stop post-Stroke Antihypertensives Collaborative Study): rationale and design. J hypertens 2005;23:455-458.
372: The ENOS Trial Investgators: Glyceryl trinitrate vs. control and continuing
vs. stopping temporarily prior antihypertensive therapy, in acute stroke:
rationale and design of the Efficacy of Nitric Oxide in Stroke (ENOS) trial.
Int J Stroke 2006;1:245-249.
ESO�̐����ł́C���@�O�ɕ��p���Ă����~���܂��p�����ׂ����ۂ��ɂ��ẴX�^���X��������Ă��܂���ł����D
COSSACS��ENOS�̌��ʂ́C2010.1.16�̎��_�ł܂����\����Ă��܂���ł����i��q�j�D
���@�O�ɓ������Ă����~���܂́C�]�����}�����Ɍp������ׂ����C���~����ׂ���
����������オ���ۂɐf�Â����Ă���Ƃ��ɕ����f�p�ȋ^��́C���@�O�ɓ������Ă����~���܂��C�]�����}�����̓��@��Ɍp���������ėǂ��̂��C���邢�͈�U�x�ׂ��Ȃ̂��C�Ƃ������Ƃł��D
�c�O�Ȃ���C�{�M�̔]�������ÃK�C�h���C��2009�ɂ��C���������ÃK�C�h���C��2009�ɂ��C���@�O�ɓ������Ă����~���܂̌p���̉ۂɂ��Ă͋L�ڂ�����܂���D
�L�ڂ��Ȃ��ƁC���悢��ǂ����Ă����̂�������Ȃ��Ȃ��Ă��܂��C�K�C�h���C���̈Ӗ�������܂���D
�������CAHA/ASA�FGuidelines for the Early Management of Adults With Ischemic
Stroke�F2007�N4���łɂ́C���@�O�ɍs���Ă����~���Ö@�̖�܂�]�������nj�24���Ԉȓ��Ɏn�߂ėǂ��Ƃ���܂��D
���̗��R�ɂ��Ă͋L�ڂ�����܂��C��ʓI�ɔ]�[�Nj}�����ɂ͌������ꎞ�I�ɏ㏸����̂ŁC����܂ō~���܂�������Ă������҂��]�����}�����ɍ~���܂��x�Ă��܂��ƁC����ɏ㏸���邱�Ƃ��\�z����܂��D
2010�N7����COSSACS�̌��ʂ����\����܂����iLancet Neurol 2010;9:767�j�D�p���̑��{��PROBE�����ŁC����48���Ԉȓ��̔]�������҂ňȑO��蕞�Ă���~���܂����̂܂܌p������̂ƁC2�T�Ԓ��~����̂Ƃ��r���������ł����D�������͎��k��������13mmHg�i95%CI
10�`17�j�C�g����������8mmHg�i95%CI 6�`10�j�ŗD�ʂɉ�����܂������Cprimary endpoit�ł���2�T�Ԍ�̎��S�ƐQ������imRS��3�j��RR
0.86�i95%CI 0.65�`1.14�Cp=0.3�j�ŗL�Ӎ��͂���܂���ł����D�������C���̌����ł́C�x�[�X���C���̌����̕��ς�149/80mmHg�Ƃ���قǍ����Ȃ����ҏW�c�ł����D
�����āC2014�N10����ENOS�̌��ʂ����\����܂����iLancet 2014 Oct 22�j�D���̌����͑��{���������ŁCpartial -factorial trial�Ƃ���RCT�ł��D����́C�����㏸���}���]�����œ��@�������҂�ΏۂɁC�j�g���O���Z�����\�t�܂��g�p���邩�ۂ��ƁC���Ƃ��ƍ~���܂�����ł������҂�ΏۂɁC���̍~���܂��p�����邩���~���邩�Ƃ���2�̉���ɂ��ē����ɒ��ׂ��Ƃ��������f�U�C���ł��D
��v�G���h�|�C���g�ł���90����̋@�\�\�㑼�C�S�ẴA�E�g�J���Ńj�g���O���Z�����\�t�܂̎g�p�͗L�ӂȉ��P�������܂���ł����iTable 3�j�D���̌����ł̃x�[�X���C���̌����̕��ς�167(SD
19)/90(13)mmHg�ƁC���݂̍~�����ÊJ�n��i�]�[�ǂ�220/120mmHg�ȏ�C�]�o����180/130mmHg�ȏ�j�����ׂ�ƁC��͂肻��قǍ����Ȃ����ҏW�c�ł����D�j�g���O���Z������\�t�����Q�ł��C1���ڂ̍~���͗ǍD�ł��C7���ڂɂȂ�Ɠ\�t���Ă��Ȃ��Q�ƂقƂ�nj����ቺ�x���ς��Ȃ��Ȃ�Ƃ��������[�����ʂł����D�]�[�Nj}�����ɂ͈�ߐ��Ɍ����������Ȃ�܂�����C�����Ȃ������������~����p������C�ϐ��������Ɏ��R�Ɍ��������������Ă���Ƃ���C���������ɕۂ�p�Ƃ��ẮC���̎�ނ̍~���܂������[�Y�i�u���ȑI���ɂȂ邩������܂���D
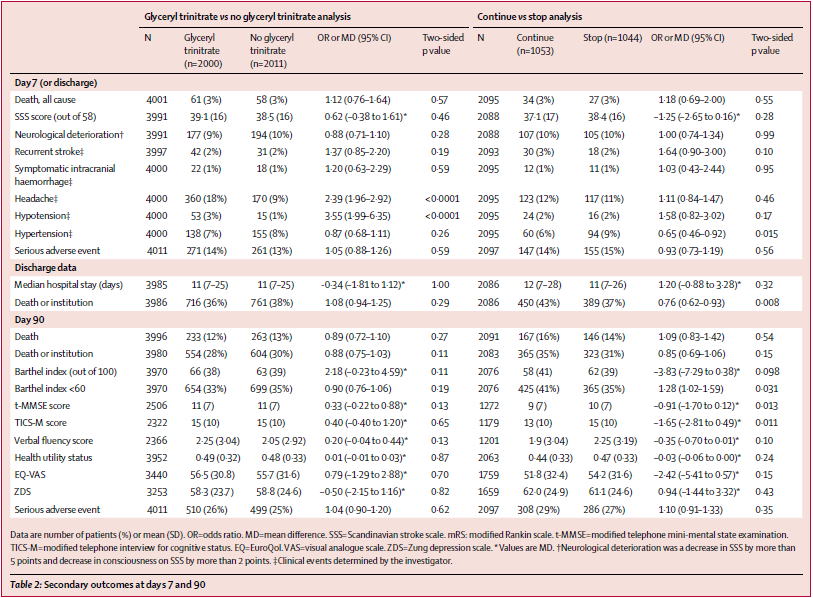
�x�[�X���C���̌����̍����Ɋւ��āC�j�g����r�ł̃T�u��́iFigure 3�j�ł́C���k��������200mmHg�ȏ�ł̓j�g�����g�������������Ƃ������ʂł��D�ł�����C�����ƌ����������W�c������I��Ŏ������s������C�������ʂ��o����������܂���D���́C������厖�Ȃ̂́C�����ƌ������Ⴂ�l�B�ł͊Q���o�邾�낤�Ɨ\�z����邱�ƂȂ̂ł����C���̌����ł�160mmHg�����ňꊇ��ɂ���Ă��܂��Ă���̂��c�O�ł��D�Ǘᐔ�̕��z�����Ă��C���̑w�������ƍׂ��������ăT�u��͂��Ă��ǂ������̂ł͂Ȃ����Ǝv���܂��D
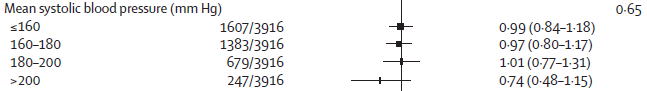
Figure 3: Subgroup analysis of eff ects on functional outcome at 90 days
for glyceryl trinitrate versus no glyceryl trinitrate�@��蔲��
����C���Ƃ��ƕ��p���Ă����~���܂𒆎~���邱�Ƃł��C�p�����ĕ��p�����ꍇ�Ɣ�r���āC��v�G���h�|�C���g�ɗL�ӂȍ��͂���܂���ł������C�@�����S��{�݂ւ̓]�@���L�ӂɌ���iOR
0.76�C95%CI 0.62�`0.93�Cp=0.008�j�C�܂��@�\�\����������܂����D�������C���p���p�������Q�ł��C����Ȃǂ̖�肪����C���ۂɌp���ł����̂�70.9%�ɗ��܂�܂����D������Q�Ȃǂŕ���ł��Ȃ��l�ł��C�o�@�݊ǂ�}������Ȃǂ��Ă����ƕ���ł��Ă�����C���ʂɍ����������\���͂���܂��D�p���Q�̕����Q�������F�m�@�\�̈�����������Ƃ������ʂł����C���̊��ҏW�c�ł̃x�[�X���C���̔�r���Ȃ��̂ŁC���Ƃ��Ƃ̔w�i���q�̈Ⴂ������\�����ے�ł��܂���D�ƂĂ��C�ɂȂ�܂��D
�ӊO�������̂́C�p�����~��r�̃T�u��́iWeb Figure 3�j�ŁC������͐�قǂƈ���Č����������قnjp�����L�v�Ƃ͂Ȃ��Ă��Ȃ��_�ł��D��{�I�Ɍ����ƃC�x���g���ǂ̊W�͊ɂ₩��J curve�����ƍl������̂ŁC���̌��ʂ͂�����Ɖ��߂ɋꂵ�݂܂��D

Web Figure 3. Functional outcome in pre-specified subgroups: continue versus
27 stop pre-stroke antihypertensive drugs.
����1�C�p���Q�̕��p�~���܂Ń��Ւf��3���ʓ����Ă���̂͂�����Ƒ����ł��D���̌����ł́C�~���܂�1�`2�g�p���S���҂�3/4���߂�̂ŁC����ł͐ϋɓI�Ƀ��Ւf�I��Ă���Ǝv���܂��D�ߔN���Ւf��͎��S���𑝂₷�\��������Ƃ��č~�����Â̑��I������O��܂������C�{�����ł̓��Ւf��p���Ă��銳�҂������������Ƃ��C���ʂ����������\���͂���Ƃ������������藧���܂��D
������ɂ��Ă��C�l�I�ɂ́CCOSSACS��ENOS�̌��ʂ���͊����̐f�ÃK�C�h���C���̋L�ڂ̒ʂ�C�]�����}�����ɂ́C�]�[�ǂȂ�Ύ��k������220mmHg�ȏ�C�]�o���Ȃ��180mmHg�ȏ��15%���x�̍~���i�]�[�ǂȂ��200mmHg���x�ȉ��ɁC�]�o���Ȃ��150mmHg���x�ȉ��ɂ��Ȃ��j�ɗ��߂邱�Ƃɕς��͂���܂���D�g�p����~���܂́C�ꖡ�̂����J���V�E���h�R����ʎ����_�H�ɂ��܂��D����Ƃ͕ʂɁC�a�i�s���ł�����Ƃ��Ɠ������Ă����~���܂͒��~�C�a���肵�Ă�����Ƃ��Ɠ������Ă����~���܂͌p���Ƃ���̂��ǂ��Ǝv���܂��E�����āC�������ɐV���ȍ~���܂��J�n����ꍇ�́CACE�j�Q�����I���ɂ��܂��D
�]�����}�����ɁC�����R���g���[���̂��߂ɐV���ɍ~����̓������n�߂�ꍇ�́C������J�n���ׂ���
���āC�]�������ÃK�C�h���C��2009�C���������ÃK�C�h���C��2009�CAHA/ASA�CESO�ƁC�����O�̔]�����֘A�K�C�h���C���ɂ����錌���R���g���[���ɂ��Ă̋L�ڂ��T�ς��Ă��܂����D
�ł́C��́C�]�����}�����̌����R���g���[�����ǂ���������̂ł��傤���D
���������ÃK�C�h���C��2009�ł̔]�������}�����̌����Ǘ��̍��ɂ́C�h�~���ẤC�ʏ픭��1�����ȍ~�̖���������J�n����D�������C�}�������Â��I������1-2�T�Ԍォ��J�n����ꍇ������D�~���ڕW�́C�N��Ȃǂ��l�����Ȃ���C���ÊJ�n��1-3���������ď��X�ɍ~�����邱�Ƃ��d�v�h�C�Ə�����Ă��܂��D
�܂�C�]�����}�����̔���1�����ォ��̍~�����Â̊J�n�����������C1�T�Ԍ�ȍ~�ł���ΊJ�n���Ă��悢�C�Ɖ��߂ł��܂��D
����3�T�Ԃ̕��͑傫���悤�ȋC�����܂����C�ǂ̂悤�ȏꍇ�ɍ~���J�n�𑁂߂�ׂ��Ȃ̂��C�K�C�h���C�������Ă�������Ȃ��i�K�C�h���Ă���Ȃ��j�Ƃ����̂́C����ォ�炷��C���Ƃ�����Ȃ��Ƃ���ł��D
�Ƃ���ŁC�����Ŗ��ɂȂ�̂́C�]�����̓��@���Ԃ́C�ʏ�2-4�T�Ԃł��邱�Ƃ��������Ƃł��D
���ɁC����1�����ȏ�o���Ă���~�����Â��J�n���悤�Ƃ���ƁC�މ@��ɂȂ�̂Ŏ��ÊJ�n���x���C���邢�͍ň��̏ꍇ���Â����т��\��������܂��D
����́C���Ɏ厡�オ�ς�����ꍇ�ɕp������ƍl�����܂��D
���������āC�����I�ɂ́C�V�K�̍~���܂͔��ǂ���1�T�Ԍ�ȍ~�̑މ@���O����J�n�����Ƃ����Ƃ���ł��傤�D
�Ȃ��C�{�M�ł��C�]�������ÃK�C�h���C��2009�̔]�������}�����̌����Ǘ��̃G�r�f���X�̍��Ɉȉ��̂悤�ȋL�ڂ�����܂��D
���G�r�f���X
�i�����j
�]�[�ǔ��nj�1���ڂ���ƁC7���ȍ~����A���M�I�e���V���U�^�C�v�T��e�̝h�R��ł���J���f�T���^���𓊗^�����Q���r����ACCESS study�ł́C1���ォ�瓊�^�����Q�̕���12������̎��S���ƌ��ǃC�x���g��L�ӂɒቺ�������D������7���ڂ܂ł̊��Ԃɒu���Ă����Q�ɂ����錌���ɍ��͂Ȃ�����9)�i�Tb�j�D
9) Schrader J, Luders S, Kulschewski A, Berger J, Zidek W, Treib J, et
al. The ACCESS Study: evaluation of Acute Candesartan Cilexetil Therapy
in Stroke Survivors. Stroke 2003;34:1699-1703 |
����́CARB�͓������J�n���Ă��~�����ʂ�����̂Ɏ��Ԃ�������̂ŁC�}��������J�n���Ă����Ɏx��͂Ȃ��Ƃ������Ƃ��Ӗ����Ă��܂��D
�{������ARB���p�����Ă���Ƃ����̂��C�}�C�`�ł����CACE�j�Q��ł������@�����l������̂ŁC���@�㑁���ɍ~�����Â��J�n���邱�Ƃ�������邩���m��܂���D
�����C�܂�����1���̌����ł���������Ă��Ȃ��̂ŁC�����_�Ŕ��Ǒ�������V���ɍ~���܂�lj�����Ƃ����̂́C�E�ݑ����Ǝv���܂��D
�܂��C�J���V�E���h�R���ACE-I/ARB�����~�����ʂ̔����������̂ŁC���@�㑁���ɍ~�����Â��J�n����ꍇ�̑I���Ƃ��ẮC������ׂ��ł��傤�D
�]�����}�����̌����Ǘ��ɂ��Ă̌��_
�]�[�Nj}�����ɂ́C����܂œ������Ă����~���܂�3�����x�x�ĕa�������Ȃ����Ƃ��m�F���Ă���ĊJ���C�V���ȍ~����́C���ǂ���2�T�Ԍ�ȍ~�i�ǂ�Ȃɑ����Ă�1�T�Ԉȍ~�j�ɊJ�n�����̂��ǂ��Ǝv���܂��D���̏ꍇ�C������Q�ɂ��x���̗\�h���ʂ����҂��āCACE�j�Q�����I���Ƃ��܂��D
�]�����}�����̌����Ǘ��ɂ��ẮC�]�������ÃK�C�h���C��2009�ł̐���
���{�������w��@���������ÃK�C�h���C��2009�iJSH2009�j�ł́C���A�a���҂ł̌����Ǘ��ɂ��Ă̐����́C�ȉ��̒ʂ�ł��D
��7�́@���������������鍂����
POINT 7a
�y���A�a�z
1�D���A�a�����������̍~���ڕW��130�^80mmHg�����Ƃ���B
2�D���A�a�������������҂ɂ�����~����I���ɍۂ��ẮC���E������ӂւ̉e���ƍ����Ǘ\�h���ʂ̗��ʂ��CACE�j�Q��CARB�����I���Ƃ��Đ�������C�����Ǘ���Ca�h�R��C���ʂ̃T�C�A�U�C�h�n���A���p�����B�܂��C�J�쐫���S�ǂ�����S�؍[�Ǎ�����ł́C���Ւf����S�ی��p��L���C�����Ǘ��Ɏg�p�\�ł���B |
�ȏ�̂悤�ɁC���A�a���҂ł́C������130/80mmHg�����ɃR���g���[������悤�ɐ�������Ă��܂��D
�������C���̊�ɂ͍���������܂���D
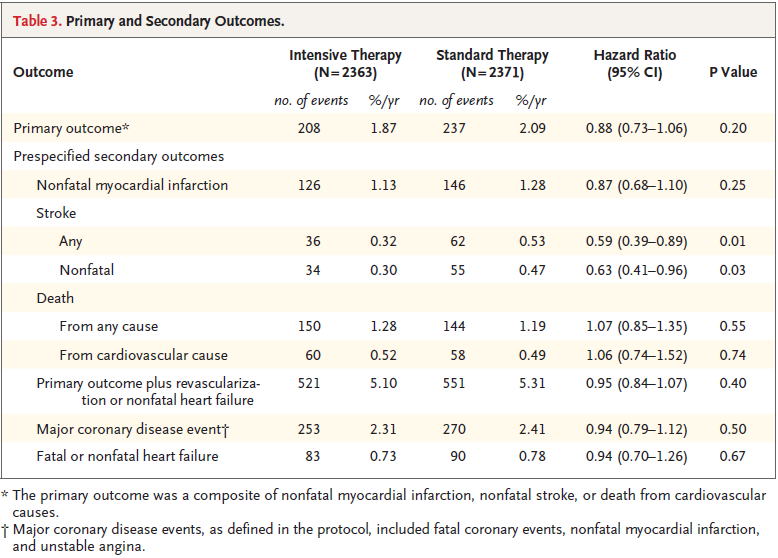
�Ƃ��낪�C����8�N�̓��A�a���҂ɑ��錵�i�Ȍ����R���g���[���Ŏ��S�����㏸����\��������Ƃ������ʂ�������ACCORD�����Ɠ����ɁC�����Ǘ���ACCORD
blood-pressure trial�iACCORD-BP�j�iN Engl J Med 2010;362:1575�j���s���܂����D���̌����͕��ϒǐՊ���4.7�N�ԂŁC��v�����S�؍[�ǁC��v�����]�����C�S���ǎ��̕����A�E�g�J�����C���k��������120mmHg�����ɊǗ�����ƔN��1.87%�C140mmHg�����ɊǗ�����ƔN��2.09%�ƁCHR 0.88�i95%CI 0.73�`1.06�j�ŗL�Ӎ����Ȃ������D�����S���C1.28%��1.19%�ƁC�L�Ӎ����Ȃ����̂�HR 1.07�i95%CI 0.85�`1.35�j�Ə㏸����\��������܂����D�]�����Ɍ��肷��ƁC�N�Ԕ��Ǘ���0.32%��0.53%�ŁCHR 0.59�i95%CI 0.39�`0.89�j�ƗL�ӂɌ������܂����D���������āC2�^���A�a���҂Ō��������i�ɃR���g���[������ړI�́C�]�����̗\�h�̂��Ƃ������ƂɂȂ�܂��D
����ɁC2012�N�Ɍ������R�z�[�g�����iBMJ 2012;345:e5567�j�����\����܂����D����́C126,092�l��18�Έȏ�̐V�K����2�^���A�a���҂�ΏƂƂ����C�M���X�̌����ŁC����3.5�N�Ԃ̒ǐՂ�20.2%�����S���C������130/80mmHg�����ɃR���g���[���������҂ł͐������̉��P�Ɗ֘A���Ȃ������Ƃ̌��ʂł����D�ނ���C�Ⴂ�����͑����S�̃��X�N�𑝂₷���ƂƊ֘A���Ă��܂����D���k��������130�`139mmHg�ŃR���g���[������Ă������҂���Ƃ���ƁC110mmHg�ŃR���g���[������Ă������҂̑����S���X�N��HR
2.79�i95%CI 1.74�`4.48�j�ƗL�ӂɏ㏸���Ă��܂����D
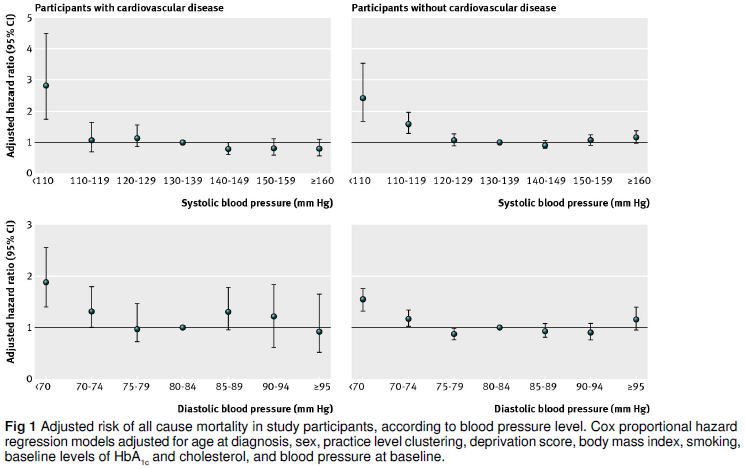
�����̌��ʂ܂��āC2013�N�N1�����č����A�a�w��iADA�j�̓��A�a���Â�Position statement�ł́C���A�a�������������҂̍~���ڕW�l��140/80mmHg�Ɉ����グ�܂����D
ACCORD-BP�̌��ʂ��炷��ƁC�]�����\�h���ʂ����҂��Ď��k��������120mmHg�����ɂ���̂��]�܂������ƂɂȂ�܂����CACCORD-BP�ł̔]�������Ǘ��͔N��0.53%����0.31%�Ɍ���Ƃ������̂ł����DADA��Position
statement�̒��ł́CACCORD-BP�ł̔]�����\�h��NNT��5�N��89�i1�N�ł�455�j�C����ɑ��Ď��_�⍂�J���E�����ǂƂ������d��ȕ���p�̔��ǂ�1.3%����3.3%�ɗL�ӂɑ������C�������NNH��5�N��50�Ɣ]�����\�h���ʂ����傫���Ȃ��Ă��܂����߁C���X�N�x�l�t�B�b�g���l�������ɂ͉���������͖̂]�܂����Ȃ��Ƃ������_�ɒB���܂����D�܂��C2012�N�ɔ��\���ꂽ2�^���A�a���҂ł̌����Ǘ��̃��^�A�i���V�X�iArch Intern Med 2012;172:1296�j�ł��C�]������35%�L�ӂɌ��炷�Ƃ���܂������C�]�������Ǘ����킸��1%�ł���C�����b�g���傫���Ȃ��Ƃ���܂����D���k������130�`139mmHg�̓��{�l�̔]�������Ǘ��́C�v�R�������iArch Intern Med 2003;163:361�j�ł�1000�l�N��12.5�Ȃ̂ŁC�N��1.25%�ƌ����܂��D��̔N��0.53%�Ɣ�r����Ɗm���ɓ��{�l�̕����]�������Ǘ��������ł����C�~���Ö@�ɂ����ʂ�ACCORD-BP�̌��ʂ���RR��0.31/0.53��0.61�Ƃ���ƁC�~�����邱�Ƃɂ��N��1.25%����N��0.76%�ɂȂ�CNNT�ɂ����1�N��435�l�ɂȂ�܂��D���̏W�c�͓��A�a���҂ƔA�a���҂̗������܂�ł���̂ŁC���A�a���҂ł̔��Ǘ����̂��̂͂��̐��l���������͂��ł����C����ł�����p�̔��Ǘ�����͏\���Ⴂ�Ƃ����܂��D�܂��C�v�R�������̃O���t������ƁC���k������130mmHg������130�`139mmHg�Ƃł͔]�[�ǔ��Ǘ��ɑ傫�ȈႢ�͂Ȃ��Ɛ�������܂��D���������āC���{�l�̔]�������Ǘ����������Ƃ𗝗R�ɍ~���ڕW��140mmHg�����łȂ��C�킴�킴130mmHg�����ɉ�����̂́C��p�Ό��ʂ��l����Ɛ������Ȃ����Ƃ�������܂��D
�v�R�������ɂ����錌���ʔ]�������Ǘ��iArch Intern Med 2003;163:361�j
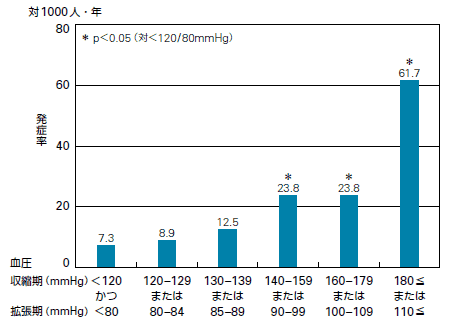
�܂����B���A�a�w��iEASD�j���C���ÊJ�n�����ƍ~���ڕW��140mmHg�i�g���������j�Ɉ����グ�܂����D�������\�肳��Ă��鉢�B�������w��/���B�S���a�w��iESH/ESC�j�K�C�h���C���ł��~���ڕW�l�̊ɘa�ɓ����Ƃ݂��Ă���C�~���ڕW���ɘa���铮���͍L�����Ă��܂��D
�ȏ���C2�^���A�a���҂ɂ����錌���Ǘ���140/90mmHg������ڕW�ɍs�����Ƃ��]�܂����C�i���{�́j�f�ÃK�C�h���C���ʂ�ɍs���ꍇ�ł��C�������Ⴍ�Ȃ�߂��Ȃ��悤�ɒ��ӂ���ׂ����Ǝv���܂��D
�@����������
 �������A���h�X�e�������@�i���ڐV��2009/10/3�C�ŏI�X�V2014/1/15�j �������A���h�X�e�������@�i���ڐV��2009/10/3�C�ŏI�X�V2014/1/15�j
�S���������҂̖�5%���������A���h�X�e�����ǂƂ����̂�����C�����ł���قǏ��Ȃ��킯�ł͂���܂���D���Ƃ����āC���������f���ɑS��j���C�A���h�X�e�����𑪒肷��Ƃ����̂́C���O�����̍�����w�a�@�������ȂȂLjꕔ�̐��a�@�łȂ������肷���ł��傤�D�S��ōR�A���h�X�e��������g��Ȃ��ƌ����R���g���[�����ł��Ȃ��킯�ł͂Ȃ��ł����C�ʏ�{�Ԑ��������ǂŗp����~���܂Ō����R���g���[�����ł���C���Â͉���ς�肠��܂���D
�����C�������A���h�X�e�����ǂƐf�f�����Ď��Â�����K�v������Ƃ���ƁC�^���ׂ���ԂƂ��ẮC�ȉ��̂悤�Ȃ��̂��������܂��D
- �^���ׂ��a��
- 40�Έȉ��Ŕ���
- ���Ò�R���i�������C�X�s�m�����N�g���͂悭�����j
- �}���Ɍ����R���g���[��������
- ��J���E�����ǁiK��3.0mEq/L�j�F�������C�������A���h�X�e�����ǂł�������K 3.5�`4.0�ł���C�����J���E���l����͈͓��ł��ے�ɂ͂Ȃ�Ȃ�
- ����
- ���{������w��iJES�j��2010�N�ɉ��������������A���h�X�e�����ǂ̐f�f���ÃK�C�h���C���ł̊
PAC/PRA��ialdosteron rennin ratio; ARR�j
�����A���h�X�e�����Z�x�iPAC�j�ƌ������j�������iPRA�j�̔�
PAC�ipg/mL�j/PRA��200
- �ȉ��̂悤�Ȋ������܂��D
PAC�ing/dL�j/PRA��20�CPAC�ing/dL�j��12����PRA��1�ŃX�N���[�j���O
��PAC�ing/dL�j/PRA��20�@�́@PAC�ipg/mL�j/PRA��200�@�Ɠ���
�����J���E���P�ƁC�����A���h�X�e�����P�Ƃ�芴�x�������C�������j�������P�Ƃ������ٓx�������Ƃ���_��������D
���x�E���ٓx�C�ޓx��͈ȉ��̒ʂ�D
�����̌����ł́C�������A���h�X�e�����ǂ̐f�f��́CPRA��1.0ng/mL/h���A��Ald��12microg/24h���A���i�g���E�����卂�l�i��200mEq/24h�j�������D
��PAC�ing/dL�j/PRA��20�@�́@PAC�ipg/mL�j/PRA��200�@�Ɠ���
��nifedipine�Ȃǂ�dihgydropyridine�n�J���V�E���h�R��g�p���ł́C�����j����A���h�X�e�����ƂȂ�̂ŁCPAC/PRA�䂪�Ⴍ�Ȃ�iJ Clin Endocrinol Metab 1997;82:457�j�D
���������āCdihgydropyridine�n�J���V�E���h�R��g�p���ł̃A���h�X�e�����ǂ̐f�f�̂��߂ɂ́C�x��2�T�Ԍ�ɑ��肷��K�v������D
���{������w��@�������A���h�X�e�����ǐf�f���ÃK�C�h���C���|2009�|��2010.4�����i��ʈ�ƌ����j�ł́C�ȉ��̎菇�Ō������A���h�X�e�����ǂ�f�f����悤�������Ă���i�ȉ��C�����j�D
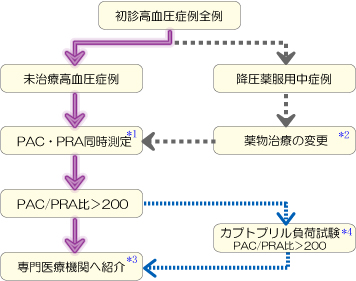
1�jPAC�EPRA��������
�@�̌��p���͍��ʂł��ǂ����C�\�ł���̌�30���ȏ�O������É�ʂ��悢�D
�@(1)PAC�F�����A���h�X�e�����Z�x�ipg/ml�j
�@�@�@�i�P�ʂɗ��ӁFng/dl�\���̍ۂ́C10�{��pg/dml�\���̐��l�ƂȂ�j
�@(2)PRA�F�������j�������ing/ml/hr�j
2�j��ܕύX
�@���A��C�A���h�X�e�����h�R�����Ւf����g�p���̏ꍇ�́C�����ɒ��ӂ����̍~����ɕύX���CPAC/PRA������s��
�@�i���A��C�A���h�X�e�����h�R���6�T�Ԉȏ�C���Ւf���2�T�Ԉȏ�O�ɒ��~����j�D
�@���̍~����Ƃ͈ȉ��Ɏ������́D
�@(1)�u�g�����W���i�u�e���W��(R)�j
�@(2)���Ւf��F�h�L�T�]�V���i�J���f�i����(R)�j�Ȃ�
�@(3)Ca�h�R��
3�jPAC/PRA�䁄200�Ő���Ë@�ւ֏Љ�
�@�J�v�g�v�������������s���ꍇ�́C�ȉ��̎菇�ōs���D
�@(1)�J�v�g�v����50mg�i�J�v�g����(R) 12.5mg 4���j���p
�@(2)���É�ʁi�܂��͍��ʁj��ۂ��C60�i90�j����ɍ̌�
�@(3)����F���p���PAC/PRA�䁄200��z���Ɣ���i�܂���PAC��120pg/ml���z���Ɣ���j |
���Ȃ낭�̋L�ړ��e�ɊԈႢ�����w�E��������₲�ӌ�����������������́C����C�������܂Ō�A���������D


Copyrights(c)2004- Eishu NANGO
All rights reserved
�֖��f�]��
|

 �iAnn Intern Med. 2017�j
�iAnn Intern Med. 2017�j
 �iJAMA. 2014;311(5):507-520�j
�iJAMA. 2014;311(5):507-520�j