|
English version is here.

アンケートにご協力を!
ご感想をお寄せ下さい
このページへリンクを張る際は,
お手数ですが
管理人までご一報ください
|
ホーム > なんごろく >
なんごろく−消化器
ヘリコバクターピロリ感染症
 ヘリコバクターピロリ菌除菌による胃癌予防 (項目新設2010/6/24,最終更新2016/3/1) ヘリコバクターピロリ菌除菌による胃癌予防 (項目新設2010/6/24,最終更新2016/3/1)
ヘリコバクターピロリ菌を除菌すると十二指腸潰瘍が8割(RR 0.20),胃潰瘍が7割(RR 0.31)防げます(CDSR 2009:CD003840).
ここで,私たちの期待は,ピロリ菌を除菌すると胃癌が防げるか,ということです.
ピロリ菌が胃癌の原因となっているのは,ほぼ正しい事実だと思います.
日本人のコホート研究(Arch Intern Med 2000;160:1962)では,年齢調整胃癌発生率は1000人年あたり男性で5.3人,女性で1.3人で,ピロリ菌抗体陽性だと男性ではRR 2.59倍年齢調整胃癌発生率が高くなりました.
ただし,この研究では,女性ではリスクにはならないという結果でした.
もう一件の胃十二指腸潰瘍,胃過形成,NUD患者を対照とした日本の後ろ向き研究(N Engl J Med 2001;345:784)では,7.8年の追跡で,ピロリ菌感染がないと胃癌発生率が0%だったのに対し,ピロリ菌感染があると2.9%でした.
それでは,ピロリ菌を除菌したら,胃癌の発生がなくせるのでしょうか.
これまで,ピロリ菌を除外することによる胃癌予防の臨床研究は何度か試みられました.
ピロリ菌除菌による胃癌発症予防の個別研究
胃癌のハイリスク患者を対象として7.5年間追跡した中国のRCT(JAMA 2004;291:187)では,発症数が少なすぎて有意差が出ませんでした.
この研究では,前癌病変のない患者では有意差があったと報告されましたが,胃癌発症数は除菌群0例,プラセボ群6例と,やはり発症数が少なかったため,意味のある有意差とは言えません.
また,7.3年間追跡した中国でのRCT(J Natl Cancer Inst 2006;98:974)では,胃癌発生が除菌群では1.68%,プラセボ群では2.39%でしたが,有意差はありませんでした.
これに対して,日本の北大第三内科浅香教授らが発表した早期胃癌治療後の患者を対象として36ヶ月追跡したRCT(Lancet 2008;372:392)では,胃癌の再発が除菌群で3.3%,対照群で8.7%と有意に減りました.
これは,ピロリ菌除菌が胃癌発生を防ぐことを証明した最初の臨床研究ということになります.
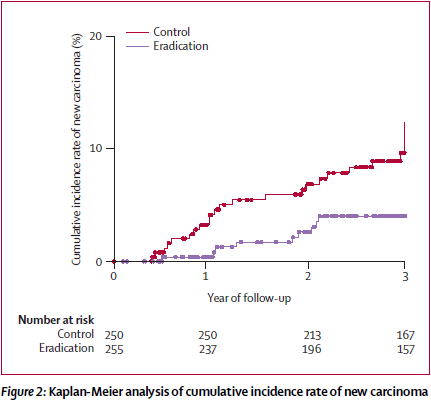
これを受けて,各種メディアにその結果が発表されました.
以下に示すのは,2008年8月1日発行の朝日新聞ですが,この記述には重大な問題があります.
Lancetに掲載された研究を受けて,ピロリ菌を除菌すると胃癌が予防できるとしていますが,本研究は内視鏡治療後の二次予防についてのものですから,この結果をもってまだ胃癌を発症していないピロリ菌保有者で除菌をしたら胃癌が予防できるかという一次予防に対しても有効かどうかは分かりません.それにもかかわらず,浅香教授の言葉として「胃潰瘍か十二指腸潰瘍の患者に限られている除菌の保険適用を,ピロリ菌感染者全体に広げ,胃がん予防に役立てるべき」と書かれています.
これは論理に大きな飛躍があり,二次予防でしか有用性が証明されていないものを,一次予防にも用いるべきとするのは,あまりに無知か意図的に除菌治療を広めたいと考えているかのいずれかと思われます.
旧帝大教授がこのような発言をすることは,社会的にインパクトが大きいので,あってはならないと思います.
この内容は,北大第3内科のサイトにも掲載されています.

2010年6月に,厚労省はピロリ菌除菌の適応を拡大することにしました.
しかし,ここには胃癌の一次予防目的でのピロリ菌除菌は適応とされていません.
これは正しく理解されている証拠ですので,除菌治療が濫用される心配がありません.
費用対効果を無視した,無謀とも言える提言は無視されたことになります.
しかし,2013年2月22日より,厚労省はピロリ菌除菌の適応をさらに拡大することにしました.慢性胃炎に対する除菌の保険適用です.初めて,胃癌の一次予防に対してピロリ菌除菌が保険適用となったことで,一線を越えてしまいました.内視鏡検査を行うことを条件としているという点では乱用を防ぐ対策がなされています.
これに対して,むしろ適用拡大は遅かったと主張する消化器内科医のブログもあります.
ピロリ菌除菌による胃癌発症予防のメタアナリシス
では,慢性胃炎患者におけるピロリ菌除菌で,本当に胃癌を予防できるのでしょうか.
2009年に発表されたピロリ菌除菌による胃癌予防のメタアナリシス(Ann Intern Med 2009;151:121)では,7件のRCTのメタアナリシスで1.7%から1.1%にRR 0.65(95%CI 0.43〜0.98)倍有意に減少したとされました.しかし,この論文に対するletter(Ann Intern Med 2009;151:513)では,Leung et al, 2004の研究とZhow, 2008の研究が酷似しており,同じ研究が二重にカウントされたものではないかと指摘しています.また,Figureにはなっていませんが,本文中には,前癌病変(=慢性胃炎)の進展に対する治療効果はRR 0.66(95%CI 0.41〜1.04)倍と有意差はありませんでした.したがって,この研究結果をもって慢性胃炎患者にピロリ菌を除菌すれば胃癌が防げるとは結論づけられません.
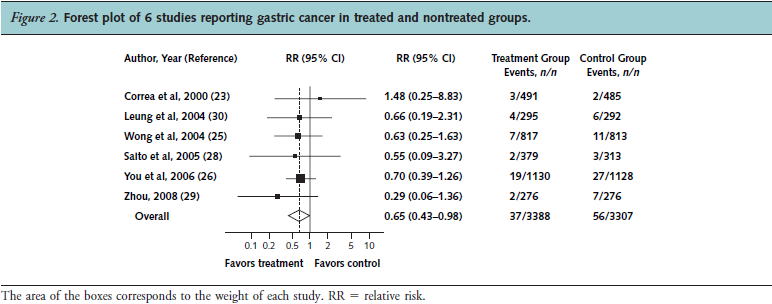
また,このメタアナリシスでは,You et al, 2006の研究(J Natl Cancer Inst 2006;98:974)が全体の占めるweightとしては突出しています.この研究では,除菌群と非除菌群の胃癌発生率は1.7%と2.4%であり,全体の1.1%と1.7%から比べると高いです.この研究の追跡期間は7.3年間なので,特別他の研究と比べて突出して長いということもありません.したがって,診断率が高いことが分かります.ただ,論文を見ても,胃癌発症率が高い理由がよく分かりません.
除菌群と非除菌群の胃癌発症数はそれぞれ19例と27例ですが,割り付けをした1142例と1143例から12例と15例脱落しています(本研究はピロリ菌除菌,ガーリック,ビタミンの3つの胃前癌病変抑制効果を検証した2×2×2 factorial designです).脱落理由が書かれていませんが,胃癌発症数に対して脱落率がそこそこ多いので,結果がひっくり返る可能性があります.
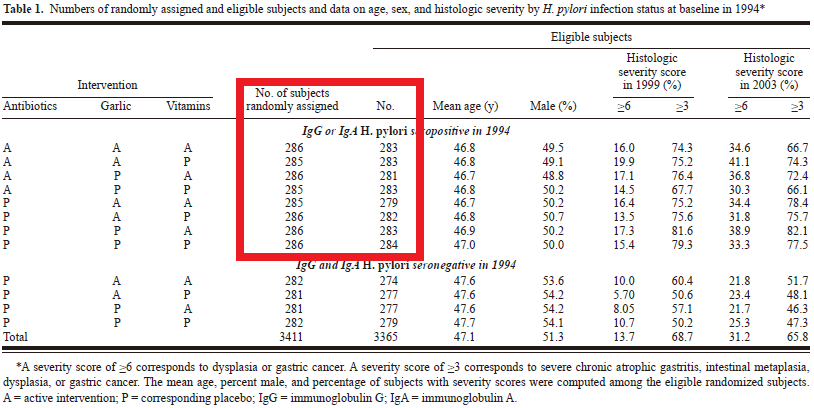
なお,この論文の本文を見ると,もともとはdysplasiaとgastric cancer(組織分類9段階中の6以上)をendpointとしていたが,胃癌だけでも効果が見られたので,そちらの結果を示したとあります.これは,selective outcome reporting bias(選択的アウトカム報告バイアス)になります.つまり,効果がなければ発表せず,効果があったので発表するというバイアスです.

さらに,2014年にBMJに無症状の健常人に対するピロリ菌除菌が胃癌を抑制できるか検証したシステマティックレビュー(BMJ 2014;348:g3174)が発表されました.
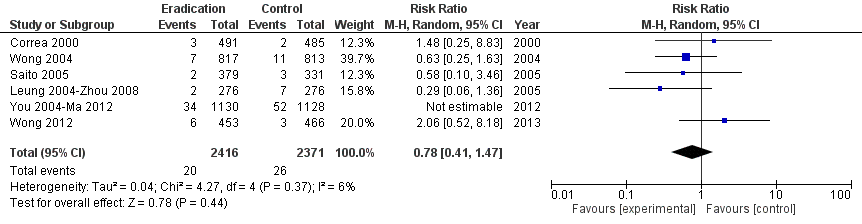
こちらでも,ピロリ菌除菌によって胃癌発症がRR 0.66(0.46〜0.95)倍減る(Fig2)という結果でした.
ただ,胃がんによる死亡はRR 0.67(0.40〜1.11)(Fig5),総死亡はRR 1.09(0.86〜1.38)(Fig6)と有意な減少は見られませんでした.
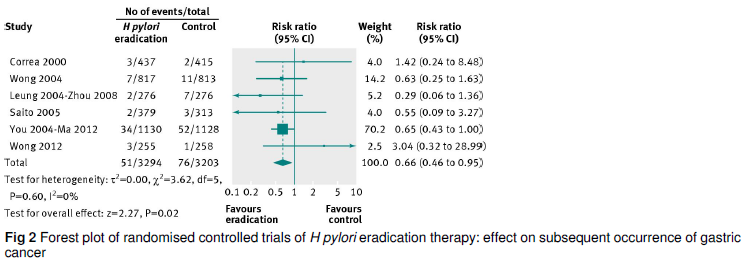
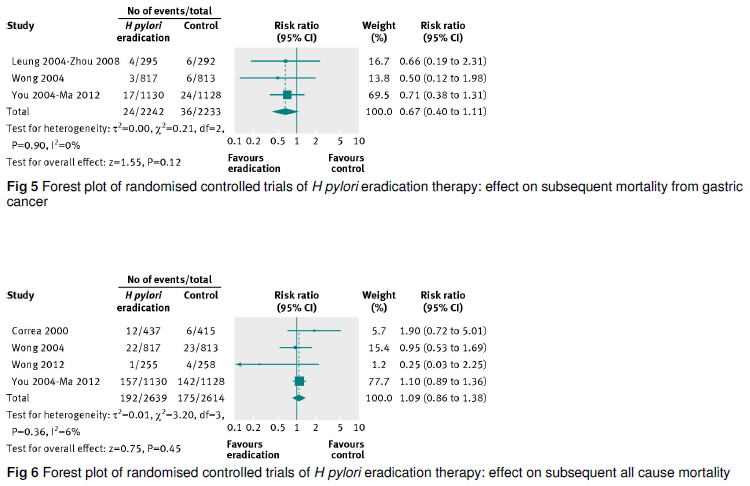
ここでも,先ほどのYou 2004の研究が大きなweightを占めています.このYou 2004の研究は,更に長期間フォローして14.7年後のデータを出しています(Ma 2012,J Natl Cancer Inst 2012;104:488).
これをみると,延長した7.4年ほどでさらに倍ほど胃癌を発症しています.
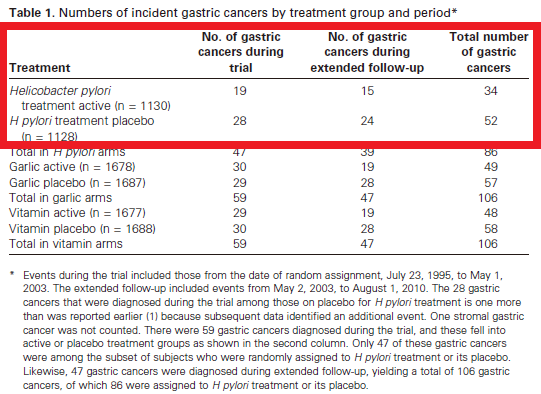
この論文で興味深いのは,supplementにあるendopoint測定の方法です.内視鏡で確認をしたのが2258例中285例しかないというのです.あとはがん登録や剖検報告などの医療記録によって調べたとあり,これでは胃癌発症数が正確には算出できません.特に除菌例では多少の症状があっても除菌しているからと内視鏡をやらないために,実際には胃癌があったとしても見逃されている可能性もあります(detection
bias).

したがって,本研究はバイアスがかかっているのでこれを取り除いて改めてメタアナリシスすると,以下のように有意差がなくなります.なお,一部データが異なりますが,ランダム割り付けされた人数をtotalの症例数としていないため,修正してあります.
そして,2015年についに,無症状の健常人に対するピロリ菌除菌が胃癌を抑制できるか検証したコクランレビュー(Cochrane Database Syst Rev 2015:CD005583)が発表されました.
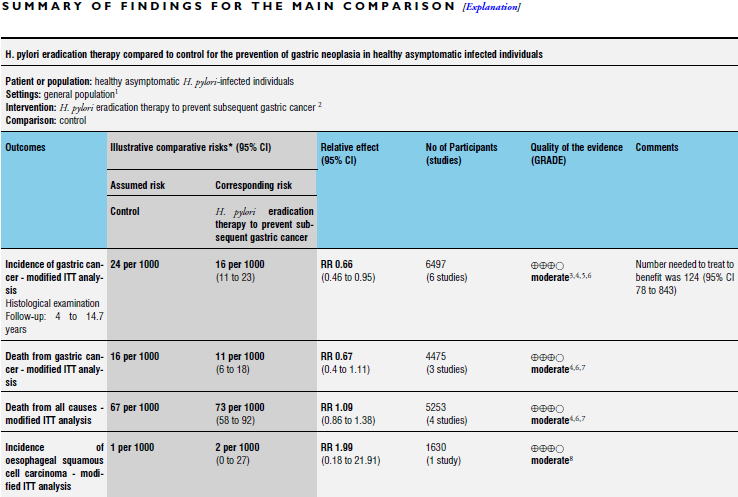
無症状のピロリ菌感染患者に対するピロリ菌除菌は,6件6,497人のメタアナリシスで胃癌発生がRR 0.66(0.46 to 0.95)倍になるというModerate Quality of the evidenceになっています.しかし,胃癌による死亡は3件4,475人のメタアナリシスでRR 0.67(0.4 to 1.11)倍というModerate Quality of the
evidenceであり,減らせるとは言えていません.さらに,総死亡に至っては4件5,253人のメタアナリシスでRR 1.09(0.86 to 1.38)倍とほとんど変わらないし,除菌による食道扁平上皮癌は1件1,630人の研究でRR 1.99(0.18 to 21.91)倍とむしろ増える傾向をしています(いずれもModerate Quality of the evidence).
つまり,ピロリ菌を除菌して,胃癌は減るかもしれないが,胃癌による死亡は減るかどうか分からず,総死亡は減るとはいえず,食道扁平上皮癌は増える可能性があるというのが,中程度の確信性を以って言えるということです.

さらに,感度分析では,もともと前癌病変がない患者ではRR 0.42(0.02 to 7.69)ですが,前癌病変のある患者ではRR 0.86(0.47
to 1.59)と効果推定値が悪いです.つまり,前癌病変のある患者には除菌をすることで胃癌予防効果は小さいし,もしかしたら効果はないかもしれないのです.
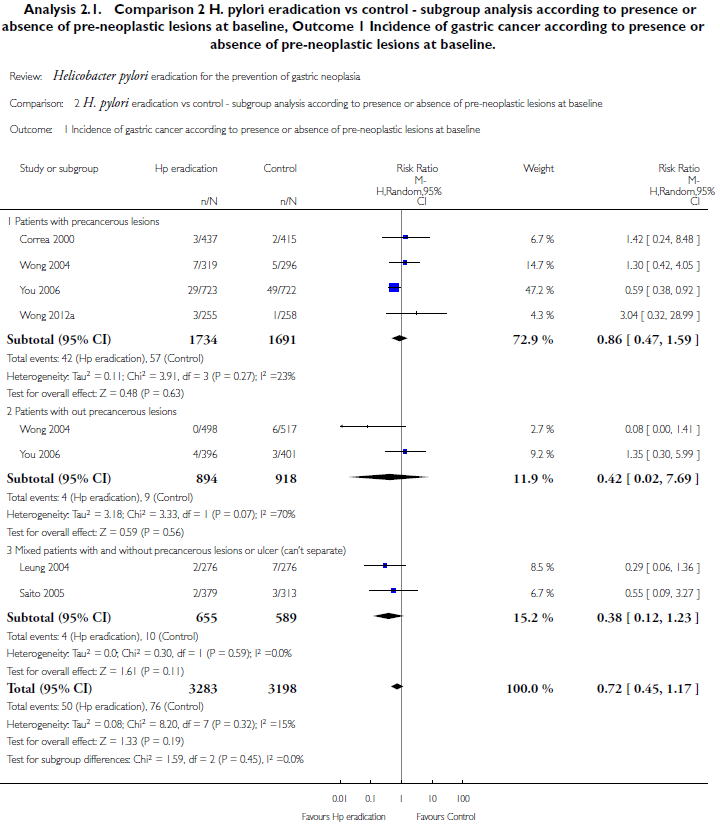
以上から,少なくとも現時点では,胃癌未発症の健常者はピロリ菌除菌によって胃癌発生を予防できるかどうか分からず,効果があるのは前癌病変を持たない患者に限定される可能性があると思います.
ピロリ菌除菌による胃癌発症予防についての結論
少なくとも現時点では,胃癌未発症の健常者はピロリ菌除菌によって胃癌発生を予防できるかどうか分からず,効果があるのは前癌病変を持たない患者に限定される可能性があります.ましてや,胃癌による死亡も,生命予後の延長も期待できません.害の可能性すらあります.
ただ,将来的に,ピロリ菌除菌によって胃癌発生を予防可能ということが明らかになる可能性はあります.
現時点での結論としては,早期胃癌治療後の患者ではピロリ菌がいれば,再発予防のために除菌をするのは勧められますが,健診でスクリーニングをしてピロリ菌感染者を見付けて全例で除菌したり,慢性胃炎患者で胃癌予防目的でピロリ除菌をする,というのは時期尚早です.
中学生に対するピロリ菌除菌事業
さらに,中学生に対してピロリ菌除菌を行って胃癌を防ぐ試みが行われています.ピロリ菌除菌による胃癌予防効果も証明されているとはいえないのに,ましてや何のエビデンスもない中学生での健診を進めようとしているのは驚きです.これは完全に勇み足です.
2015年2月8日に開催した岡山CASPワークショップで中学生にピロリ菌検診を行うべきかというワークショップを行いました.その時のプレゼンスライドを供覧します.
 ピロリ菌除菌の害
ピロリ菌除菌の害
除菌によって逆流性食道炎が起こりやすくなるといわれていました.ただ,これは現在では否定されているようです.
7件のRCTと5件のコホート研究のシステマティックレビューで,除菌と除菌後のGERD発症は関連がなかったとありました(Am J Gastroenterol 2010;105:1007).ところが,消化性潰瘍の患者に限ると,OR 2.04(1.08〜3.85)倍に増えるという結果でした.
また,ピロリ菌は免疫を司るT細胞のTh1の反応を亢進させて,Th2の反応を鈍くするため,Th2の反応によって誘発される喘息やアトピー性皮膚炎を抑える効果があるとされています(J Asthma Allergy 2010;3:139).実際に,ピロリ菌保有者でアトピー性皮膚炎が少ないという結果もあります(J Epidemiol Community Health 2007;61:638).
胃薬
胃薬で消化性潰瘍予防効果があるのは,ピロリ菌除菌,PPI,H2ブロッカー(H2RA),ミソプロストールだけです.しかし,PPIは以下のリスク増やすと言われています.
- 肺炎
- 骨折
- クロストリジウム・ディフィシル感染
- CKD
- 認知機能障害
- 死亡
また,小腸からの鉄やビタミンB12,マグネシウムの吸収障害があると言われています.さらに,クロピドグレル(プラビックス(R))と併用するとPPIがCYP2C19で代謝されるためにクロピドグレルの効果を減弱することも指摘されています.安易に漫然とPPIを処方し続けることは,厳に慎むべきです.
 PPIとH2ブロッカーによる肺炎のリスク (項目新設2010/6/25,最終更新2016/11/16) PPIとH2ブロッカーによる肺炎のリスク (項目新設2010/6/25,最終更新2016/11/16)
個別研究
コホート内症例対照研究(Ann Intern Med
2008;149:391)において,PPIを使用した場合の市中肺炎発症の調整済みオッズ比は,使用開始2日以内の場合6.53(3.95-10.80),7日以内の場合3.79(2.66-5.42),14日以内の場合3.21(2.46-4.18)でした.
症例対照研究のシステマティックレビュー(Aliment Pharmacol Ther 2010;31:1165)では,PPIの使用は市中肺炎のリスクをOR 1.36(1.12〜1.65)倍増やすことが示されました.
サブグループ解析では,短期間のPPI使用で市中肺炎の発症がOR 1.92(1.40〜2.63)倍有意に増加しましたが,慢性的なPPI使用ではOR
1.11(0.9〜1.38)と有意な増加は示されませんでした.
市中肺炎による入院歴のある65歳以上の高齢者を対象にしたコホート内症例対照研究(Am J Med 2010;123:47)でも,PPI/H2ブロッカー使用者は肺炎の再発が調整OR 1.5(1.1〜2.1)倍になることが示されました.
院内肺炎の発症にも,PPIがリスクになることも指摘されています.
入院3日目以降に発症した肺炎についてのコホート研究(JAMA 2009;301:2120)では,PPIを内服しているとOR 1.3(1.1〜1.4)倍増えることが示されましたが,H2ブロッカーでは,有意な増加は示されませんでした.
2011年のシステマティックレビュー
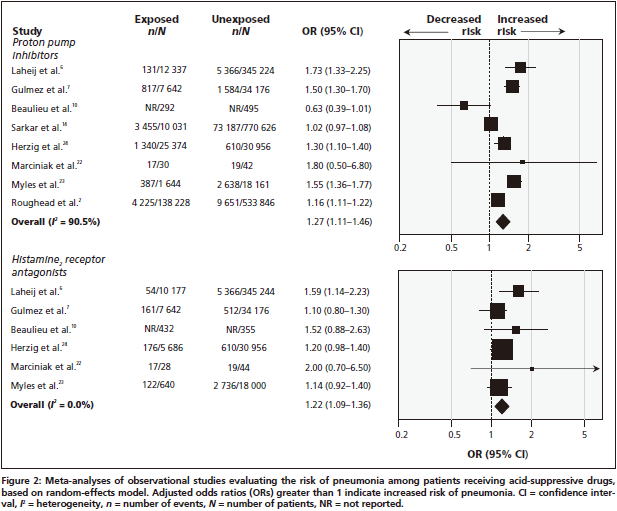
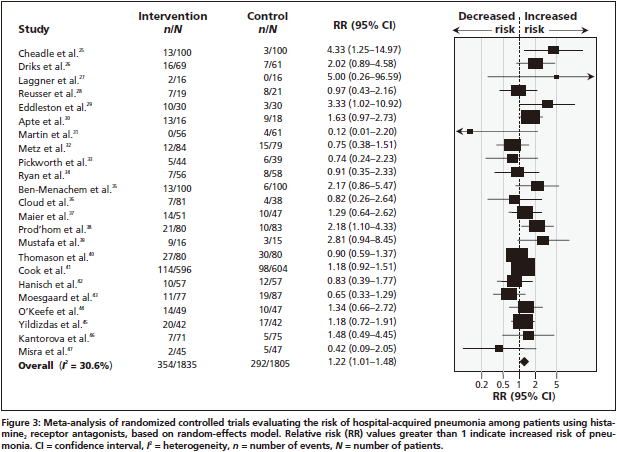
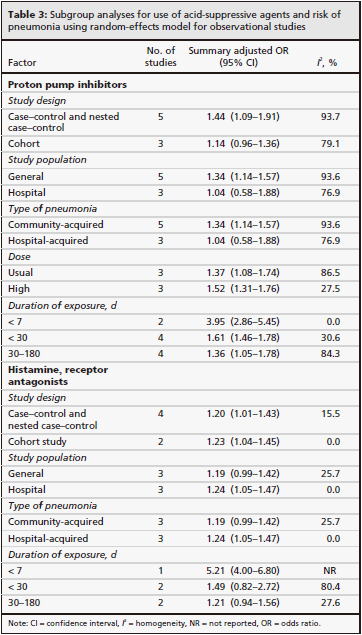
2011年に制酸剤による肺炎リスクのシステマティックレビュー(CMAJ 2011;183:310)が発表されました.5件の症例対照研究,3件のコホート研究,23件のRCTが集められ,PPIについては,8件の観察研究(症例対照研究5件,コホート研究3件)のメタアナリシスで調整済みOR 1.27(95%CI 1.11〜1.46)倍肺炎のリスクが高いという結果でした.一方,H2ブロッカーについては,6件の観察研究(症例対照研究4件,コホート研究2件)のメタアナリシスで調整済みOR 1.22(95%CI
1.09〜1.36)と,やはり有意に肺炎のリスクが高いという結果でした.H2ブロッカーについては,23件のRCTのメタアナリシスでもRR 1.22(95%
CI 1.01〜1.48)倍院内肺炎のリスクが高くなりました.
サブ解析の結果を見ると,高用量の方が低用量よりもリスクは高く,服用開始からの期間が短いほどリスクが高いという結果でした.
ところが,2013年に発表された後ろ向きコホート研究(J Gen Intern Med 2013;28:223)では,確かにPPI使用で市中肺炎の発症が増加しましたが,同時に,胸痛,変形性関節症,尿路感染症もPPI使用の方が多く発症したことから,交絡因子があるだろうと結論付けられていました.
2014年のシステマティックレビュー
また,2014年に発表された8件のコホート研究のシステマティックレビュー(Gut 2014;63:552,CNODES)でも,6カ月の観察期間では,PPI,H2RAともに肺炎の発症を増やしませんでした(PPI:aOR 1.05(95%CI 0.89〜1.25),H2RA:aOR
0.95(95%CI 0.75〜1.21)).過去のシステマティックレビューの結果との不一致について,この論文のディスカッションでは,PPIを使用した患者ではGERDが多く,GERD自体が肺炎のリスクになっているために交絡していることがPPIの見かけ上の肺炎リスク上昇を生んでいると指摘していました.
しかし,先にも述べたように,PPIによる肺炎のリスク増加は,服用開始直後に見られ(特に最初の1週間),急速に関連がなくなっていきます.6ヶ月の観察期間では,最初の1週間〜1ヶ月の害は打ち消されてしまうので,差が出なくなっても当然です.本研究での結果をもってPPIは肺炎のリスクを上げないとはいえません.せめて,投与期間別の解析を行うべきでした.
2015年のシステマティックレビュー
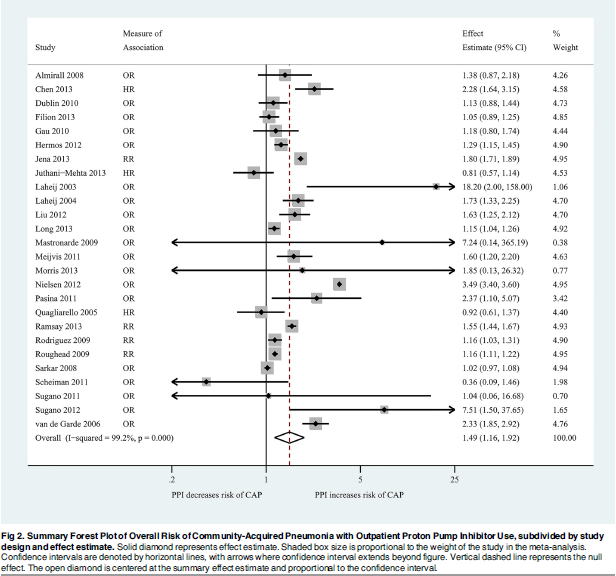
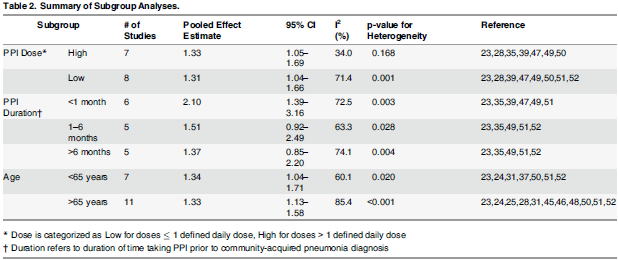
2015年に発表されたシステマティックレビュー(PLoS One 2015;10:e0128004)では,26件の研究(11件の症例対照研究,10件のコホート研究,1件のケースクロスオーバー研究,4件のRCT),6,351,656人のメタアナリシスで,外来PPI使用は肺炎をRR 1.49(95%CI 1.16〜1.92,I2=99.2%)倍増やしました.
肺炎による入院も,16件の研究のメタアナリシスでRR 1.61(95%CI 1.12〜2.31,I2=99.3%)倍でした.
H2RAによる肺炎のリスクは,8件の研究のメタアナリシスでRR 1.00(95%CI 0.90〜1.12,I2=33.7%)と有意な増加は認めませんでした.
サブグループ解析では,PPIの用量と年齢で肺炎のリスクは関係なく,PPIの使用期間が短いほどリスクが高いという従来と同様の結果を示しています.
PPIによる肺炎増加は交絡因子による影響かも
2016年に発表されたコホート研究(BMJ 2016;355:i5813)では,16万人の英国のプライマリ・ケアのカルテ調査で,PPI使用による市中肺炎リスク上昇は調整済みでHR1.67(1.55〜1.79)でしたが,同一患者でPPI使用前と使用後で比較すると,PPI使用はprior
event rate ratio 0.91(0.83〜0.99)とむしろ低くなり,PPI使用による市中肺炎増加は交絡因子の影響と考えられるとしています.
結論
結論としては,現時点では,PPIやH2ブロッカーの制酸剤は,使用開始後に肺炎発症のリスクになるため,安易な使用は控えるべきです.
ただ,リスクとなるのは,使用開始直後で,30日以上継続的に使用している患者の場合では,リスクは減ると考えられます.
※制酸剤と肺炎のリスクについては,第4回エビマヨの会(2009年6月10日)も参照のこと.
 PPIは骨折を増やす (項目新設2013/4/8,最終更新2016/4/5) PPIは骨折を増やす (項目新設2013/4/8,最終更新2016/4/5)
PPIの制酸作用により消化管内のpHが上昇した結果カルシウム吸収が減り,破骨細胞の活動性が抑制されることにより,骨密度が低くなることが示唆されています.
個別研究
高齢者を対象としたコホート内症例対照研究(JAMA 2006;296:2947)では,1年以上のPPI使用で,大腿骨頚部骨折がAdjusted OR 1.44(1.30〜1.59)倍増加しました.高用量PPIではAdjusted OR 2.65(1.80〜3.90)倍に増加しました.また投与期間でも1年で1.22(1.15〜1.30),2年で1.41(1.28〜1.56),3年で1.54(1.37〜1.73),4年で1.59(1.39〜1.80)と投与期間が長いほど大腿骨頚部骨折のリスクが増加するという結果でした.
2011年のシステマティックレビュー
PPIの骨折増加の副作用については,2011年に2件の観察研究のシステマティックレビューが発表されています.
1つ目は11件の観察研究(5件の症例対照研究,3件のコホート内症例対照研究,3件のコホート研究)のシステマティックレビュー(Ann Fam Med 2011;9:257)で,10件の研究のメタアナリシスの結果,PPIの長期使用によって全骨折がOR 1.29倍(95%CI 1.18〜1.41)増え,9件の研究のメタアナリシスの結果,大腿骨頚部骨折はOR 1.34倍(95%CI 1.09〜1.66)増え,3件の研究のメタアナリシスの結果,椎骨骨折はOR 1.56倍(95%CI 1.31〜1.85)増えたという結果でした.H2RAでは,増える傾向にありましたが,有意差はありませんでした.ただし,これらのメタアナリシスでは異質性が高く,研究間のばらつきが大きかったと考えられます.質が高い研究のメタアナリシスだと害が大きく出ていて,投与量が多いほどリスクが上がるが,男女差はないというサブループ解析の結果でした.
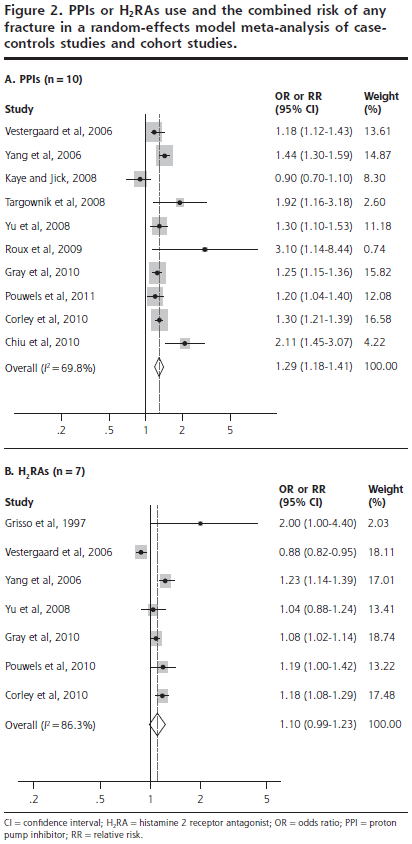
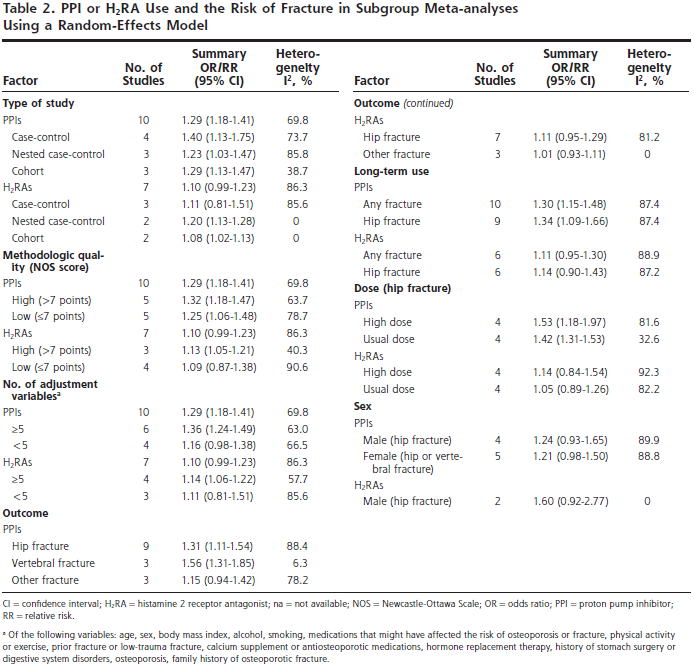
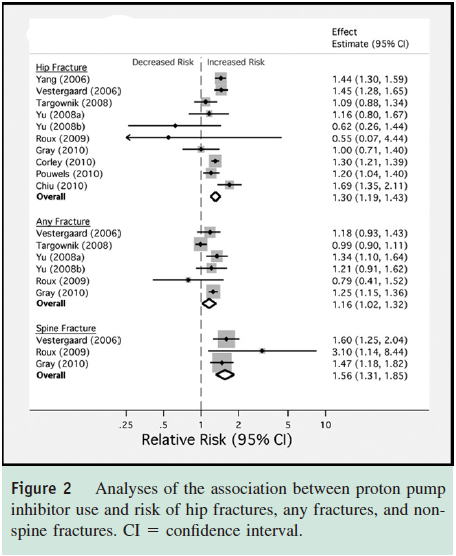
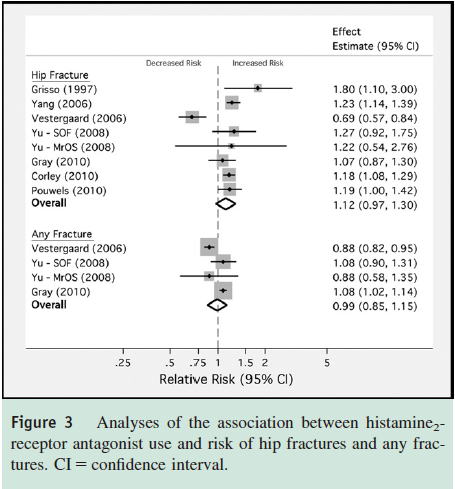
2つ目のシステマティックレビュー(Am J Med 2011;124:519)は11件の観察研究(8件の症例対照研究,4件のコホート研究)がメタアナリシスされ,PPIの長期使用によって大腿骨頚部骨折がOR 1.30倍(95%CI 1.19〜1.43)増え(10研究),全骨折はOR 1.16倍(95%CI 1.02〜1.32)増え(6研究),椎骨骨折はOR 1.56倍(95%CI 1.31〜1.85)増えた(3研究)という結果でした.H2RAでは有意な差はありませんでした.
2015年のシステマティックレビュー
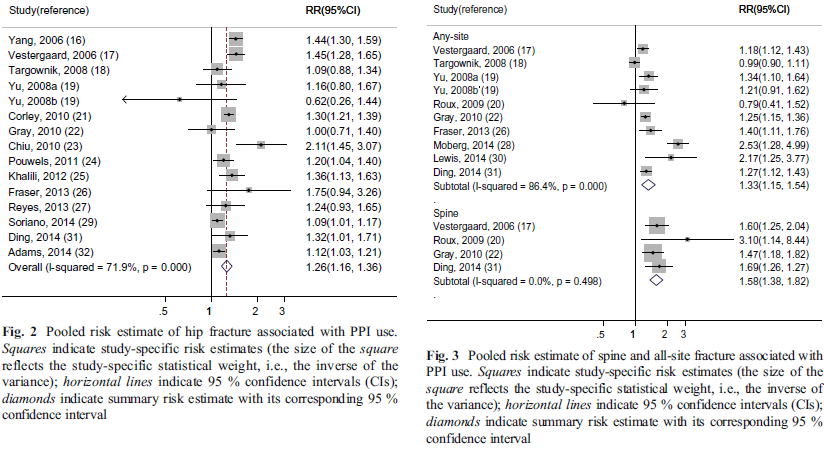
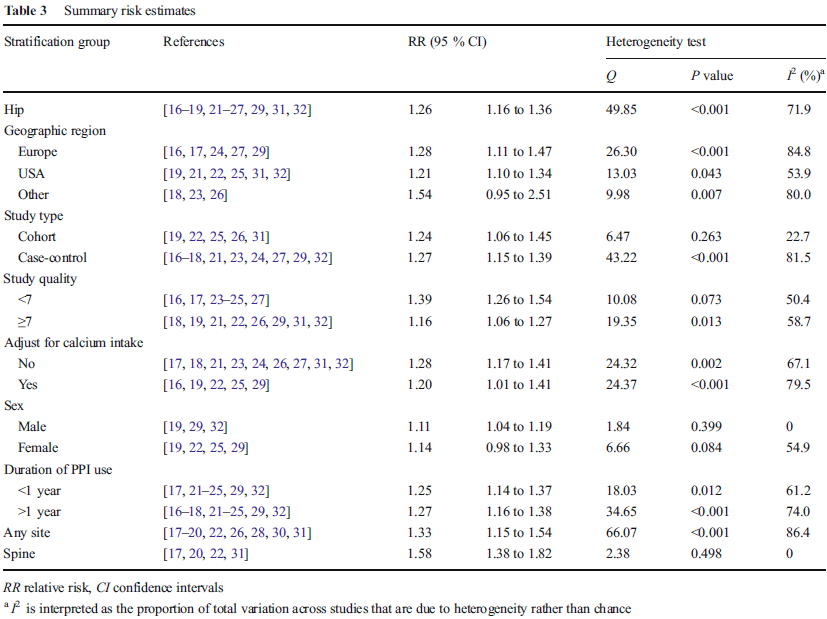
さらに,2015年には18件の研究,244,109人の患者を集めたメタアナリシスのデータが示されました(Osteoporos Int 2016;27:339).
これによれば,大腿骨頚部骨折はRR 1.26(95%CI 1.16〜1.36,I2=71.9%),全骨折はRR 1.33(95%CI 1.15〜1.54,I2=86.4%),椎体骨折はRR 1.58(95%CI 1.38〜1.82,I2=0.0%)といずれも増加しました.
サブ解析を見てみると,研究の質が高い場合にややリスクが減る(RR 1.39 vs 1.16)印象はあるものの,それ以外はサブグループ間の違いは見られませんでした.肺炎と違って,PPIの使用期間によるリスクの違いは見られませんでした.
結論
このように,PPIの長期使用によって概ね大腿骨頚部骨折は1.3倍に,椎骨骨折はOR 1.5倍増えると言えるでしょう.特に高齢者で転倒リスクが高い患者に漫然とPPIが使われるのは危険であり,厳に慎むべきだということが分かります.
 クロストリジウム・ディフィシルClostridium difficile Infection: CDIに対するPPIの害 (項目新設2017/6/16) クロストリジウム・ディフィシルClostridium difficile Infection: CDIに対するPPIの害 (項目新設2017/6/16)
個別研究
近年,PPIによってクロストリジウム・ディフィシル感染が増えるという研究が相次いで出され,トピックスになっています.984人のクロストリジウム・ディフィシル市中感染の子供と成人のコホート研究(JAMA Intern Med 2013;173:1359)では,27.7%でPPIが使われていました.驚くべきことに,感染している患者の18.0%は感染前に医療機関を受診したことがなく,35.9%には抗菌薬の使用歴がありませんでした.
システマティックレビュー
クロストリジウム・ディフィシル感染に対するPPIの影響については2007〜2013年に相次いで5件のシステマティックレビュー,メタアナリシスが発表されました.
最も大規模なものは,42件の観察研究(30件の症例対照研究,12件のコホート研究)で313,000人のデータを集めたシステマティックレビュー(Am J Gastroenterol 2012;107:1011)で,39件の研究のメタアナリシスの結果,PPI使用によってクロストリジウム・ディフィシル感染がOR 1.74倍(95%CI 1.47〜2.85)増え,3件の研究のメタアナリシスの結果,クロストリジウム・ディフィシル再発はOR 2.51倍(95%CI 1.16〜5.44)増えたという結果でした.併用例を除いた,PPI単独使用の場合はOR 2.10倍(95%CI 1.66〜2.66)に,H2RA単独使用ではOR 1.50倍(95%CI 1.23〜1.83)と,PPIの方がリスクが高いという結果でした.また,PPIと抗菌薬併用では,OR 3.87倍(95%CI 2.28〜6.56)と増加していましたが,PPI単独で抗菌薬非使用であっても,OR 1.98(95%CI 1.39〜2.83)と有意に増えました.以上より,PPIはクロストリジウム・ディフィシル感染の独立した危険因子といえます.
他の4件のシステマティックレビュー,メタアナリシス(Clin Gastroenterol Hepatol 2012;10:225,Am J Gastroenterol 2007;102:2047,PLoS One 2012;7:e50836,Am J Gastroenterol 2012;107:1001)でも,同様の結果でした.
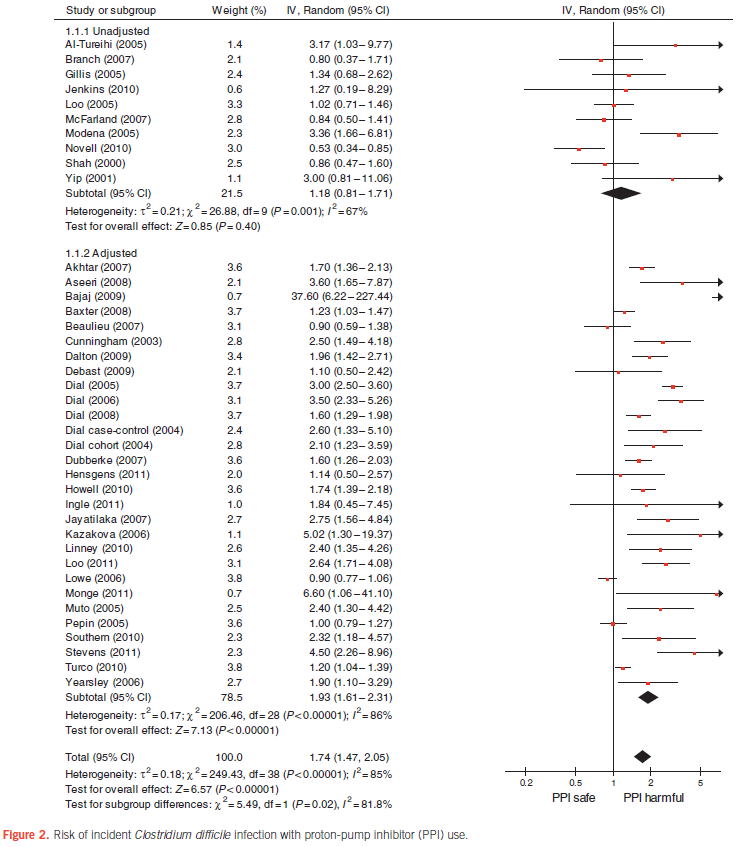
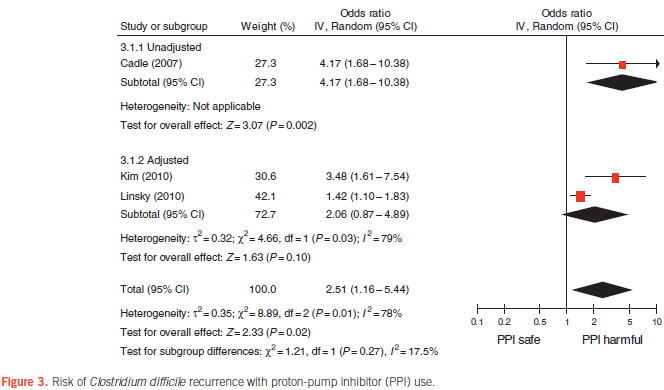
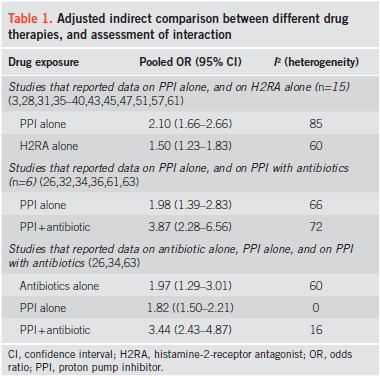
さらに,2017年に16件7703人の観察研究のシステマティックレビュー(JAMA 2017;177:784)が発表され,やはり同様に制酸剤を使用している患者はCD感染症が17.3%から22.1%にOR 1.52(1.20〜1.94)倍多いという結果でした..
 PPIはCKDを増やす (項目新設2016/4/5) PPIはCKDを増やす (項目新設2016/4/5)
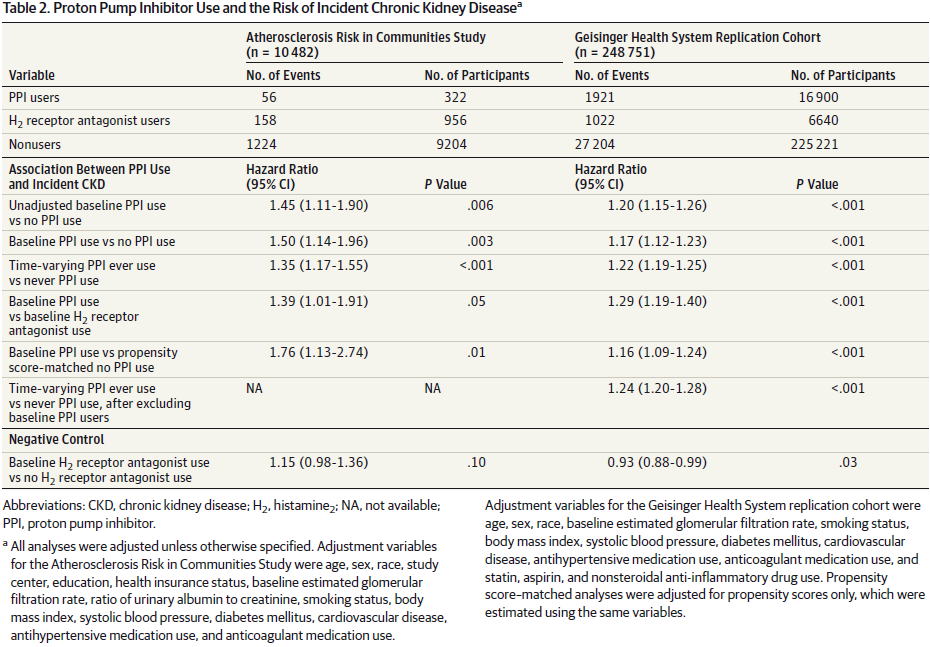
PPIの害が注目される中,2016年にPPIがCKDを増やすいというコホート研究(JAMA Intern Med 2016;176:238)の結果が発表されました.
この研究では,2つのコホートを対象に解析が行われていて,10,482人の腎機能が正常(eGFR≧60 mL/min/1.73m2)な患者を対象とした観察期間の中央値が13.9年の研究と,248, 751人の腎機能正常患者を対象とした観察期間の中央値が6.2年の研究です.
これによると,PPI使用によりCKDはおおよそ1.2〜1.4倍多く起こると言えます.
 PPIは認知症を増やす (項目新設2016/4/5) PPIは認知症を増やす (項目新設2016/4/5)
PPI使用により認知症が増えるという衝撃の結果が出ました.
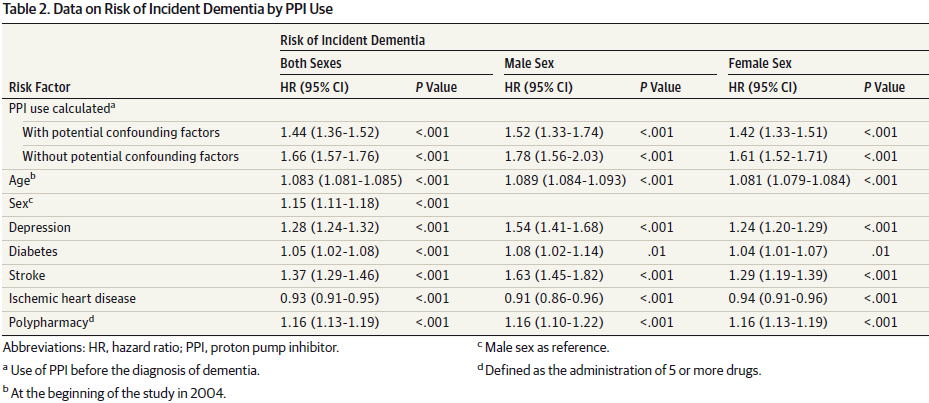
ドイツで行われた75歳以上の高齢者を対象としたコホート研究(JAMA Neurol 2016)で,PPI使用により認知症がHR 1.44(95%CI 1.26〜1.52)倍に,男性では1.52(95%CI 1.33〜1.74)倍,女性では1.42(95%CI
1.33〜1.51)倍多く起こっていました.
この研究では,年齢,うつ病,糖尿病,脳梗塞,虚血性心疾患,5剤以上のポリファーマシーも認知症のリスクになっているという結果でした.
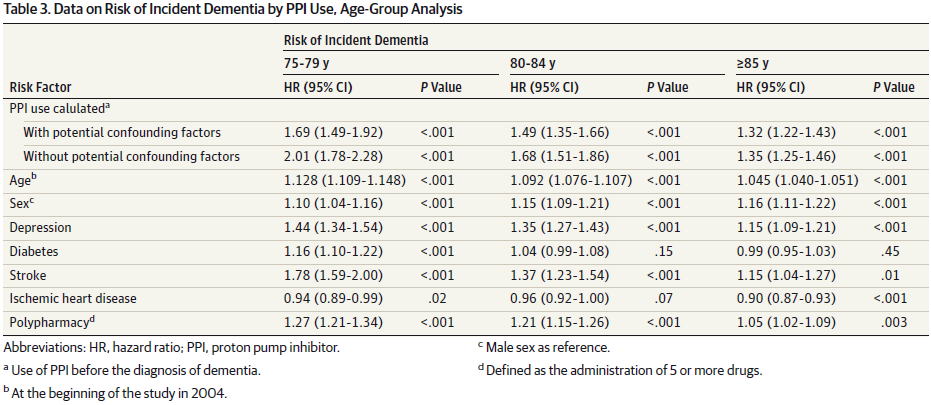
年齢別で見ると,若い人ほどPPI使用による認知症発症リスクは高い傾向が見られます.
 PPI心筋梗塞や脳梗塞を増やす (項目新設2017/5/21) PPI心筋梗塞や脳梗塞を増やす (項目新設2017/5/21)
PPIは心血管疾患を増やす
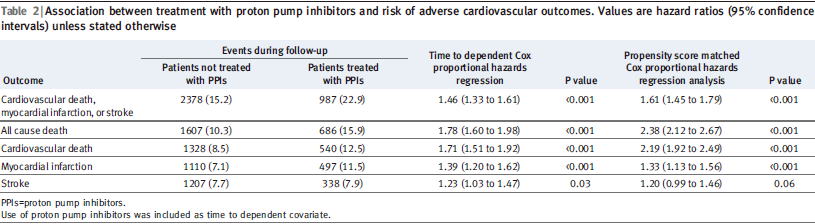
2010年のAnnals of Internal Medicineに発表されたコホート研究(Ann Intern Med 2010;153:378)はデンマークの全病院を対象として1年間追跡され,PPIの使用によって心血管イベント(HR 1.29,1.17〜1.42),総死亡(HR 1.75,1.53〜1.99),心血管死亡(HR 1.57,1.36〜1.82),心筋梗塞(HR
1.19,1.05〜1.35),脳卒中(HR 1.43,1.19〜1.71)のすべてが増えることが示されました.
PPIは全て同様にリスクを上げましたが,H2ブロッカーはリスクを上げませんでした.
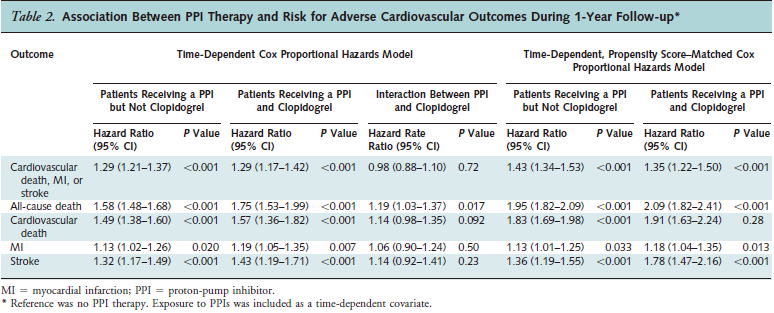
同様の結果は2011年のBMJにも1年間のコホート研究(BMJ 2011;342:d2690)が発表されており,,PPIの使用によって総死亡(HR 1.78,0.60〜1.98),心血管死亡(HR 1.71,1.51〜1.92),心筋梗塞(HR 1.39,1.20〜1.62),脳卒中(HR
1.23,1.03〜1.47)のすべてが増えることが示されました.
興味深いことは,clopidogrelの併用の有無で,心筋梗塞と脳卒中は変わりませんが,総死亡と心血管死亡はclopidogrelを併用していた方がPPI使用によるリスクがより高まるという結果だったことです.
これらの結果は,8,437人ずつを対象としたpropensity score-matchingによる解析でも同様でした.
PPIは心筋梗塞を増やす
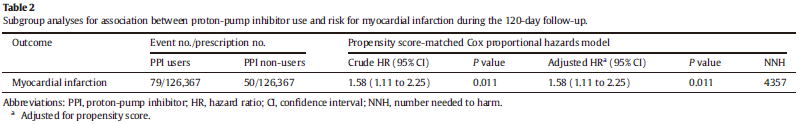
2014年に発表された台湾で行われたコホート研究(Int J Cardiol 2014;177:292)は健康保険データベースを用いた大規模な研究であり,propensity scoer-matched analysisにより126,367人ずつの患者データの解析により,PPIの使用によって心筋梗塞による入院がaHR 1.58(1.11〜2.25)倍増えることが示されました.
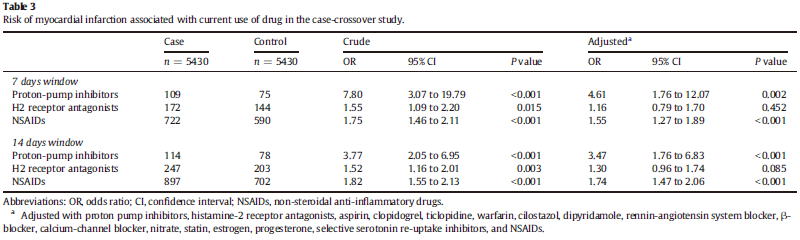
また,propensity score-matched studyでは,起点から7日以内にPPIを使用していた患者は8〜14日前に使用していた患者と比較してaOR 4.61(1.76〜12.07)倍心筋梗塞の発症リスクが高いという結果でした.NSAIDsも同様にaOR 1.55(1.27〜1.89)とリスクが高かったですが,H2ブロッカーはaHR 1.16(079〜1.70)と変わりませんでした.
PPIは脳梗塞を増やす
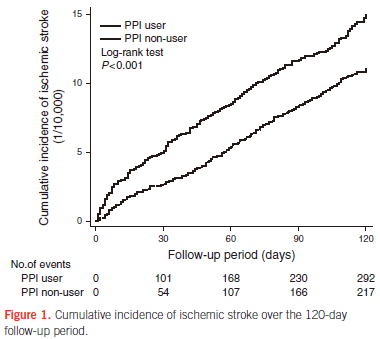
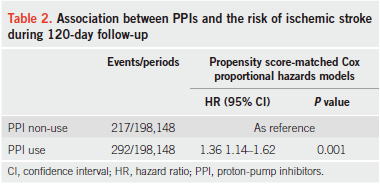
2017年に発表されたデンマークの全病院を対象としたレジストリを用いた120日間のコホート研究(Am J Gastroenterol 2017; doi: 10.1038)も患者数が多く,propensity scoer-matched analysisにより198,148人ずつの患者データの解析により,PPIの使用によって脳梗塞による入院がaHR 1.36(1.14〜1.620)倍増えることが示されました.
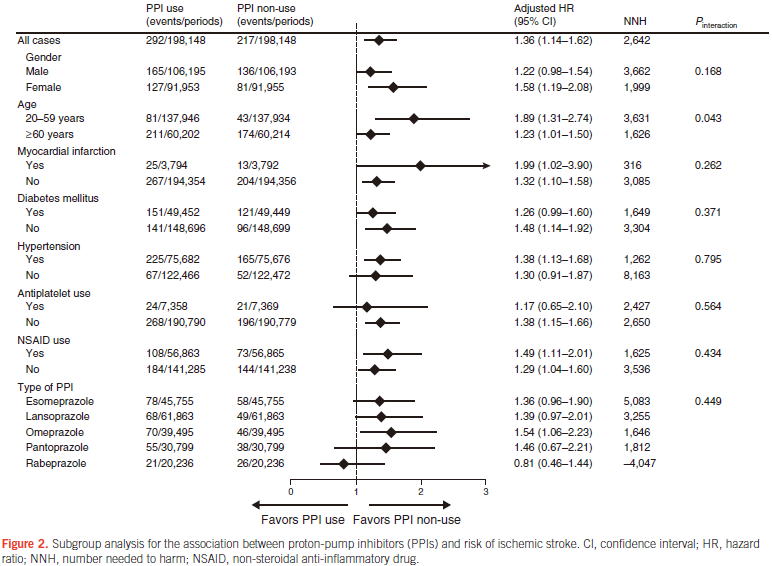
サブ解析を見てみると,年齢のみ交互作用の検定で有意差があり(P=0.043),20〜59歳のaHR 1.89(1.31〜2.74)と60歳以上のaHR
1.23(1.01〜1.50)の間に違いがあって若年者のほうがPPIによって脳梗塞を起こすリスクが高いことが示されています.
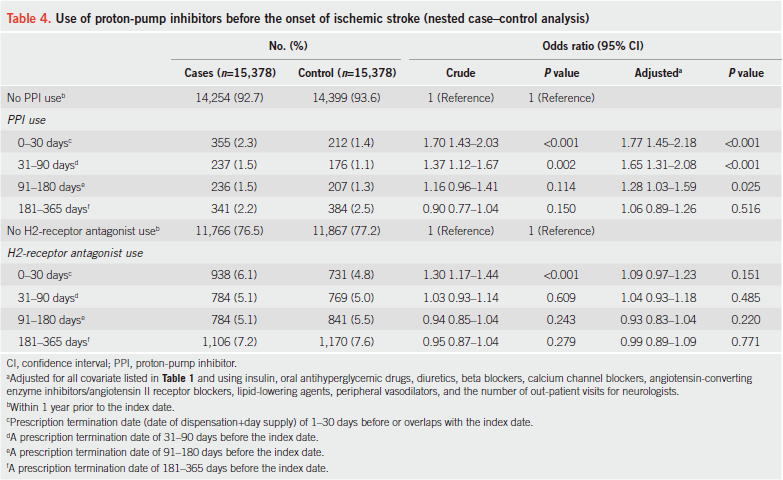
また,15,378人ずつのコホート内症例対照研究では,PPI使用は0〜30日だとaOR 1.77(1.45〜2.18)と最も脳梗塞のリスクが高く,PPIの脳梗塞発症リスクは使用日数が長くなるに連れて経時的に減ってくることが示されています.180日以上使用すればリスクは有意差がなくなります.
 PPIが死亡を増やす (項目新設2018/7/1) PPIが死亡を増やす (項目新設2018/7/1)
そしてなんと,PPIにより死亡リスクが上がるという結果が出ました.
イタリアで入院患者を対象として行われたコホート研究(JAMA Intern Med 2013;173:518)では,PPI使用は退院1年後の死亡をAdjusted HR 1.51(1.03〜2.77)倍有意に増やすとされました.特に低用量では有意差はありませんでしたが,高用量では,Adjusted
HR 2.59(1.22〜7.16)倍有意に増加しました.
なおこの研究ではPPIの高用量は,omeprazole 40mg/day,pantoprazole 40mg/day,lansoprazole
30mg/day,rabeprazole 20mg/day,esomeprazole 40mg/dayとしています.
2016年にもう1本,PPI使用者のほうが脂肪が多かったというコホート研究(BMJ Open 2016;7:e015735)が発表されました.PPIとH2RAの新規使用(349,312例),PPI使用と非使用(3,288,092例),PPIとPPI非使用・H2RA非使用(2,887,030例)を対象とした,巨大なコホート研究です.
中央値5.71年の追跡で,PPI使用はH2RAと比較してHR 1.25(1.23〜1.28)倍死亡が多いという結果でした.さまざまな方法で解析しても結果は同様で,PPIの使用期間と死亡リスクに段階的な関連がありました.
 PPIの使用・中止に対する考え方 (項目新設2015/9/30,最終更新2016/12/7) PPIの使用・中止に対する考え方 (項目新設2015/9/30,最終更新2016/12/7)
PPIは非常に有用な薬剤です.消化性潰瘍治療薬としてはピロリ菌除菌とともに最も有効な薬剤ですし,消化管出血がある場合には投与が必須です.
しかし,GERDやNUDに対して乱用されるようになり漫然と使用されている例が少なくありません.特に,胃潰瘍では8週間まで,十二指腸では6週間までしか保険診療では認められていないにもかかわらず,「難治性逆流性食道炎」と保険病名をつけて長期処方されている例が少なくありません.
また抗血小板薬の処方増加にともなって顕在化した消化管副作用の予防のためと,抗血小板薬を使用する際にはルーチンでPPIも併用するべきであると主張する人もいます.
しかし,PPIには肺炎,骨折,クロストリジウム・ディフィシル感染,死亡を増やすリスクがあることを忘れてはなりません.また,小腸からの鉄やビタミンB12,マグネシウムの吸収障害があると言われています.さらに,クロピドグレル(プラビックス(R))と併用するとPPIがCYP2C19で代謝されるためにクロピドグレルの効果を減弱することも指摘されています.安易に漫然とPPIを処方し続けることは,厳に慎むべきです.
では,PPIは止めていいのでしょうか.
先に述べたように,PPIは非常に有用な薬剤です.抗血小板薬に併用してPPIを使用していた人が中止したあとで出血性胃潰瘍を起こす例も散見されます.ですから,一律ルーチンで併用するとか,一切併用しないとかではなく,消化管出血のリスク評価を行ってPPIを併用するかどうか決めるべきです.
American College of Gastroenterology (ACG)の2009年の診療ガイドライン(Am J Gastroenterol 2009;103:728)では,NSAIDsによる消化管毒性リスクについて以下のようにリスク分類されています(ピロリ菌はこれとは別扱いにリスク因子とされています).
- 高リスク
- 中リスク(以下が1〜2項目該当)
- 年齢>65歳
- NSAIDs高用量使用
- 非複雑性の消化性潰瘍の既往
- アスピリン(低用量を含む),副腎皮質ステロイド,抗凝固療法の併用
- 低リスク
これは,50歳以上の変形性関節症と関節リウマチ患者にNSAIDsを投与した3つのRCT,34,701人のの分析(Aliment Pharmacol Ther 2010;32:1240)から得られた結果を元にしています.それによれば,それぞれの因子の出血,穿孔,閉塞,潰瘍のリスクは以下のようになります.
- 年齢≧65歳 :HR 2.25(95%CI 1.84〜2.76)
- 過去のイベント既往 :HR 2.57(95%CI 1.94〜3.39)
- 低用量アスピリン :HR 2.34(95%CI 1.87〜2.92)
- 副腎皮質ステロイド :HR 1.85(95%CI 1.41〜2.43)
これを元にした,上記診療ガイドラインでの治療の推奨は以下のようになっています.
| |
消化管リスク |
| 低リスク |
中リスク |
高リスク |
| 心血管リスクが低い |
NSAID単独
(なるべく軽い薬を少量で) |
NSAID+PPI/misoprostol |
他の治療法が可能ならばそちらを行う
または,COX2選択阻害薬+PPI/misoprostol |
心血管リスクが高い
(低用量アスピリンが必要) |
Naproxen+PPI/misoprostol |
Naproxen+PPI/misoprostol |
NSAIDsとCOX2選択阻害薬を避け,代替治療を行う |
ただ,この評価では,PPIの害を考慮した使用推奨になっていません.あくまで,消化器専門医と循環器専門医からの視点での推奨であり,十分とはいえません.
アスピリンによる出血リスクの増加
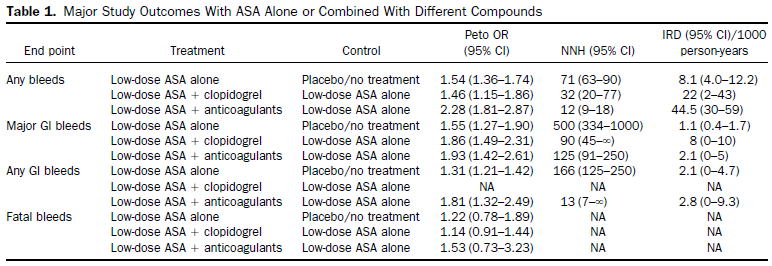
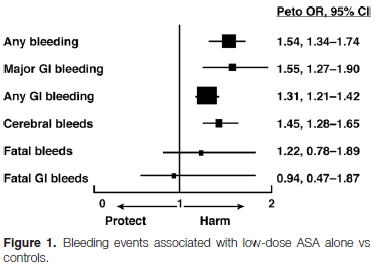
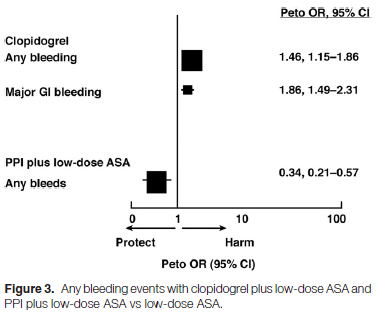
35件の低用量アスピリン単独,18件の抗凝固療法との併用,5件のクロピドグレルとの併用,3件のPPIとの併用のRCTのメタアナリシスを行った2011年のシステマティックレビュー(Clin Gastroenterol Hepatol 2011;9:762)では,低用量アスピリン単独では,全出血がプラセボ/無治療と比較して,OR 1.54倍(95%CI 1.36〜1.74)増えるという結果でした.IRD(incidence rate difference)が8.1(95%CI 4.0〜12.2)/1000人年なので,年率0.8%の絶対差として,低用量アスピリン使用により全出血のリスクが年率1.48%から年率2.28%に増加すると逆算できます.
PPIによる潰瘍,出血リスクの軽減
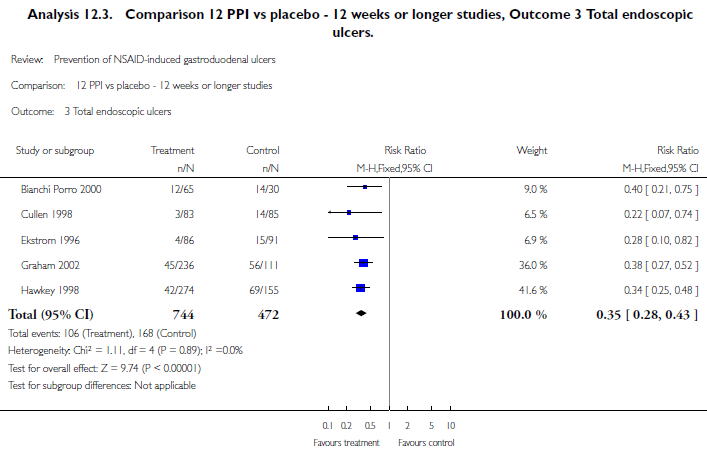
2002年(2011年のupdateでは結論変わらず)のコクランレビュー(Cochrane Database Syst Rev 2002:CD002296)では,5件のRCTのメタアナリシスで,PPIは12週以上の長期投与で内視鏡的消化性潰瘍の発症をRR 0.35倍(95%CI 0.28〜0.43)に減らしました.
また集中治療患者におけるPPIの消化管出血リスク軽減効果については,2013年のシステマティックレビュー(Crit Care Med 2013;41:693)で12件のRCT,1614人のメタアナリシスで,PPIはH2RAと比較して消化管出血リスクをRR 0.36倍(95%CI 0.19〜0.68)倍に減らしました.
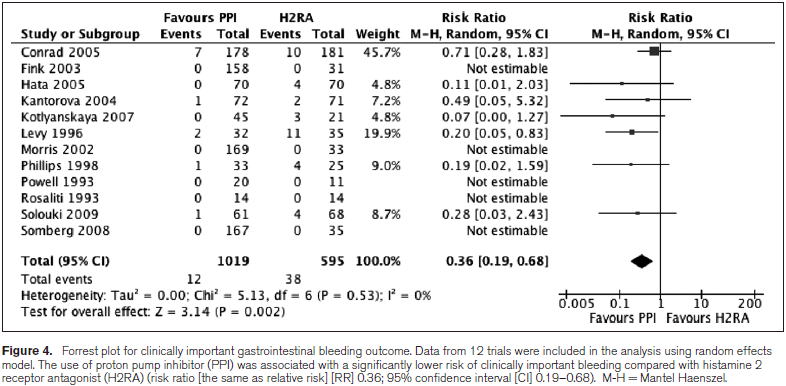
以上より,PPIを使用するとおよそ消化性潰瘍や出血は1/3に減るといえます.
PPI使用・中止にあたっての原則
以上より,抗血小板薬や抗凝固薬に胃薬を併用するか否か,著者は以下の基準で考えます.
少なくとも,アスピリン使用全例にPPIを併用するのは過剰処方です.
| アクティブな潰瘍や出血がある |
→PPIを併用する |
| アクティブな潰瘍や出血がない |
以下の出血のリスクファクターのいずれかがある
- 消化管出血の既往がある
- アスピリン(低用量を含む),抗凝固療法,副腎皮質ステロイドを併用している
- 経口摂取できず,経鼻胃管で腸溶錠ではなくアスピリン末を使用している
- 集中治療を受けている(特に人工呼吸管理中)である
|
下記のPPIの害のリスクファクターが全てない |
以下のPPIの害のリスクファクターのいずれかがある
- 肺炎の既往があるか,そのリスクが高い
- 骨折の既往があるか,そのリスクが高い
- クロストリジウム・ディフィシル感染の既往がある
|
→H2RAを併用する |
| 上記の出血のリスクファクターが全てない(抗血小板薬や抗凝固薬,副腎皮質ステロイドの単剤使用を含む) |
→PPI,H2RAともに併用しない |
PPIのdeprescribing protocol
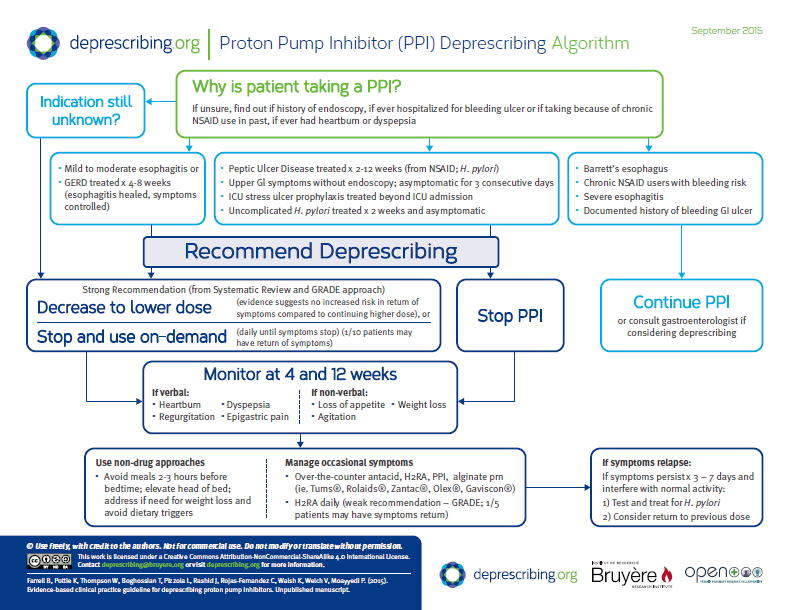
2015年9月,カナダのBruyere Research Instituteが運営するdeprescribing.orgがPPIの中止のプロトコールが発表しました.これは,高齢者の多剤併用に対する対策として,さまざまな減薬プロトコールを提案しています.その作成にあたってはGRADE
approachが用いられています.
その中に,PPIの減薬プロトコールがあります.大変シンプルで使いやすいので,紹介します.
なお,このアルゴリズムでは,PPIを継続するのは以下の場合に限られています(アルゴリズム右).
・バレット食道
・出血リスクのある慢性NSAIDs使用
・重度食道炎
・出血性消化性潰瘍の記録された既往
GERDは継続処方の適応ではないことに注意(食道炎の内視鏡所見がない上部消化管症状は,連続3日間症状が消失したら中止)
クロストリジウム・ディフィシル感染
 クロストリジウム・ディフィシル感染に対するCDトキシンの診断能 (項目新設2016/11/24,最終更新2016/11/24) クロストリジウム・ディフィシル感染に対するCDトキシンの診断能 (項目新設2016/11/24,最終更新2016/11/24)
2015年のJAMAに掲載されたシステマティックレビュー(JAMA 2015;313:398)では,CDトキシンの感度・特異度は73%と98%と感度が低いです.
感度が低い場合には繰り返し行うことにより感度を上げることができます.結核菌検査の三連痰や大腸がん検診の便潜血検査2回法とかがそれに当たります.しかし,検査を行う場合には,感度・特異度,尤度比だけでなく,事前確率も大きく影響します.
では,CDトキシンの検査は何回やればいいのでしょうか.
先程のJAMAのシステマティックレビューの結果から,CDトキシンは感度73%,特異度98%,陽性尤度比37,陰性尤度比0.28になります.さまざまな事前確率において,CDトキシンを1〜3回行った際の事後確率を考えます.事前確率10%の時の1回の検査で陰性だった場合の事後確率は3%です.3回やって3回とも陰性の場合の事後確率は0.3%です.同様にいろいろな事前確率で見てみると,以下のようになります.
| 事前確率 |
事後確率 |
| 1回陰性 |
2回陰性 |
3回陰性 |
| 10% |
3% |
0.9% |
0.3% |
| 30% |
10.7% |
3.2% |
0.9% |
| 50% |
21.9% |
7.3% |
2.2% |
| 80% |
52.8% |
23.9% |
8.1% |
つまり,事前確率80%であれば,3回陰性であってもなかなか否定しにくいですが,事前確率が10%であれば1回でも十分否定が可能ということになります(事前確率10%の1回陰性のほうが事前確率80%の3回陰性よりも可能性が低い)).これは,例えば抗菌薬治療中に下痢を発症した入院患者と外来で診る下痢患者の違いのようなものです.
藤本先生の感染症レジデントマニュアルには,toxin A/Bが陰性のとき,繰り返して検査を提出する意義はない,と書かれています.2010年のIDSAの診療ガイドラインにも「12. Repeat testing during the same episode of diarrhea is of limited
value and should be discouraged (B-II).」とあり,繰り返し検査をすることは限定的な効果しかないので行うべきではないと書かれています.
CDトキシンの感度の低さを補うのがGDHです.先の昨年のJAMAでは,GDHは感度92%,特異度93%,陽性尤度比13,陰性尤度比0.09でした.CDトキシンと比較すると感度がよく,特異度が劣ります.
現在では2-step法でキットが売りだされていて保険収載もされているので,便利ですね.となると,感度の高いGDHを組み合わせていれば,余計に検査は1回だけでよいですね.
その他
 便潜血反応(FOBT)陽性の場合に上部消化管内視鏡検査(GF)を行うべきか (項目新設2017/12/21) 便潜血反応(FOBT)陽性の場合に上部消化管内視鏡検査(GF)を行うべきか (項目新設2017/12/21)
大腸癌スクリーニング検査である便潜血反応(FOBT)が陽性の場合に,通常は下部消化管内視鏡検査(CF)を行います.では,上部消化管内視鏡(GF)を行うべきでしょうか.FOBT(+)でもCFで出血の原因となる疾患が見つからないこともありますが,上部消化管からの出血でもFOBT(+)となるという話もあり,実際のところはっきりしません.
2010年にカナダからSR/診療ガイドラインが出されていました(Can J Gastroenterol 2010;24:113).
システマティックレビューの結果,FOBT(+)/CF(-)を対象としてGFを施行した観察研究が9件あり,うち3件では胃癌は見つからず,胃癌が見つかった4件のうち3件では1%未満,1件では7%あったが14例中1例と症例数が少なく,残り2件では胃癌の有無は報告されていないという結果でした.FOBT(+)と関連するその他の胃疾患は11〜21%で見つかったが,FOBT(+)とは関係なく見つかったと判断された胃疾患も10〜36%あったとのことです.症状の有無と所見の発見率とは関連は見られなかったというのも注目するべきです.根拠に乏しいので推奨は作れず,現場で個別に判断するようにと書かれています.
9件の研究のまとめがTable 2に示されています.メタアナリシスはされていませんが,これを見ると,全体的に症例数が少ないですが,確かにFOBT(+)でCFで病変が見つなからなかった人に胃癌が存在するのは1%未満です.胃癌以外の胃疾患(消化性潰瘍など)がそれなりに見つかっているので,GFを行っても良いと思いますが,FOBT(+)と関連のない疾患を発見することも多く,過剰診断を生む可能性はあります.
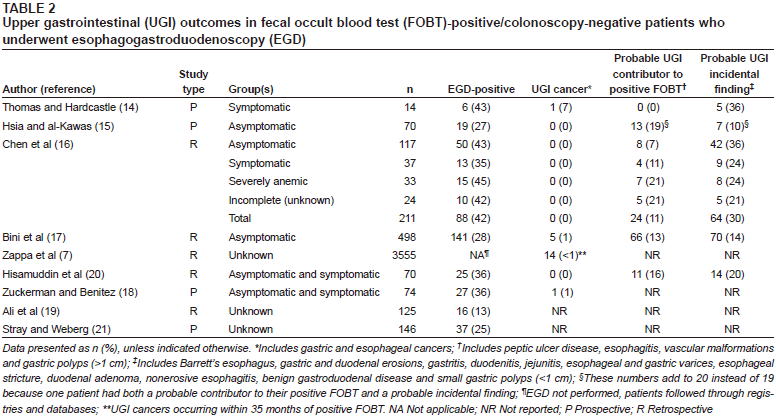
その後2013年にもう1件後ろ向き研究の結果(Scand J Gastroenterol 2013;48:657)が発表されており,やはりFOBT(+)/CF(-)患者でGFを行うと胃癌は1%,消化性潰瘍は16%見つかったと似たような結果が出ています.
以上から,FOBTは下部消化管からの出血を反映するものなので,CFで見つからなかったら小腸からの出血を考えるべきで,FOBT(+)という結果に対してはGFは原則不要だけれど,しばらくGFをやっていない人だったら,リスク評価をした上で,この機会にやるかどうか患者と相談するという方針で良いと思います.
※なんごろくの記載内容に間違いをご指摘頂ける方やご意見をお寄せいただける方は,是非,こちらまで御連絡下さい.


Copyrights(c)2004- Eishu NANGO
All rights reserved
禁無断転載
|

















































