English version is here.
このページへリンクを張る際は,
Amazon.co.jp ウィジェット
ホーム > なんごろく > なんごろく−糖尿病 >
なんごろく−糖尿病 EMPA-REG OUTCOME
Zinman B, Wanner C, Lachin JM, Fitchett D, Bluhmki E, Hantel S, Mattheus
M, Devins T, Johansen OE, Woerle HJ, Broedl UC, Inzucchi SE, for the EMPA-REG
OUTCOME Investigators.
チェックシート は はじめてトライアルシート6.2
背景: 心血管リスクの高い2型糖尿病患者に対するSGLT-2阻害薬の心血管疾患と死亡に対する効果はまだ明らかになっていない.
カテゴリー: 予防 資金源: 利益相反: Dr. Wanner reports grant support from the European Foundation of Studies in Diabetes (EFSD)/Boehringer Ingelheim European Diabetes Research Programme outside the submitted work. Dr. Hantel reports personal fees from Boehringer Ingelheim outside the
submitted work. Boehringer Ingelheim, Eli Lilly , Novo Nordisk, Abbott, Merck and Sanofi
have provided CME funding to Dr. Inzucchi's employer, Yale University. 臨床試験登録:
1.論文のPICO: P: 2 の成人(≧18歳)の2型糖尿病患者2 ,減量手術,血液疾患,癌既往,治療薬の禁忌,抗肥満薬使用,全身ステロイド使用,甲状腺ホルモン使用量調整中,不安定な内分泌疾患,妊婦・授乳婦,アルコール依存・薬物依存,他研究に参加中,臨床的に具合が悪い,急性冠症候群・脳卒中・TIAI: C: O: 本研究は,非劣性試験として計画された.
2.ランダム割付けされているか?: 2 ),居住地(北米+オーストラリア,ニュージーランド,ラテンアメリカ,ヨーロッパ,アフリカ,アジア)3.Baselineは同等か?: 診断からの年数: 10年 vs 10年 baseline A1c: 平均8.3±1.1% vs 8.3±1.1%,中央値8.1 vs 8.1 4-1.ITT解析か?: 4-2.結果に影響を及ぼすほどの脱落があるか?:
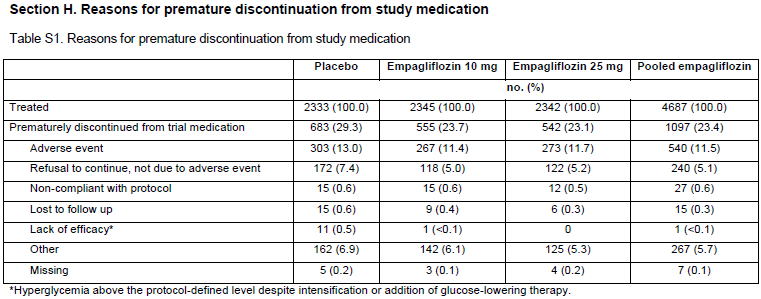
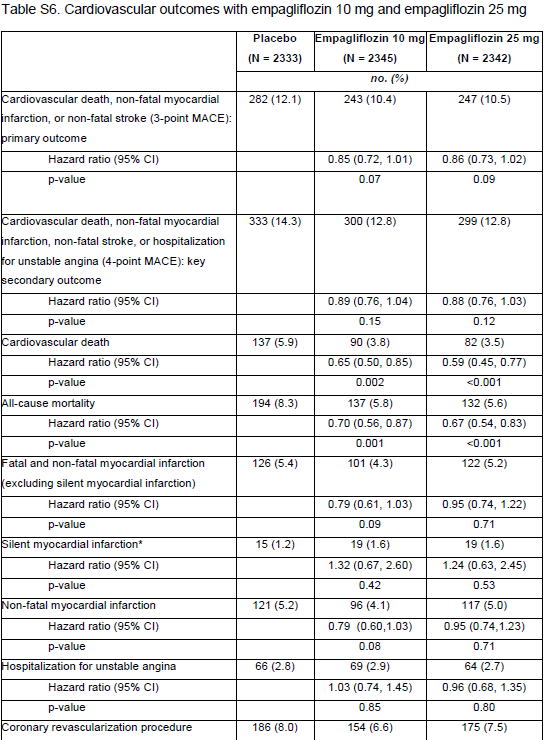
5.マスキング(盲検化)されているか?: 6.症例数は十分か?: HR 1.3をマージン とした非劣性であることだった.7.結果の評価: メインとなる結果はTable1にある. Placebo群:12.1% HR 0.86(95%CI 0.74〜0.99) ,非劣性<0.001,優越性 0.04 Placebo群:14.3% Empagliflozin群: 12.8% HR 0.89(95%CI 0.78〜1.01) ,非劣性<0.001,優越性 0.08
その他のアウトカム総死亡: 8.3% vs 5.7%,HR 0.68(0.57〜0.82),p<0.001 心不全による入院: 4.1% vs 2.7%,HR 0.65(95%CI 0.50〜0.85),p=0.002
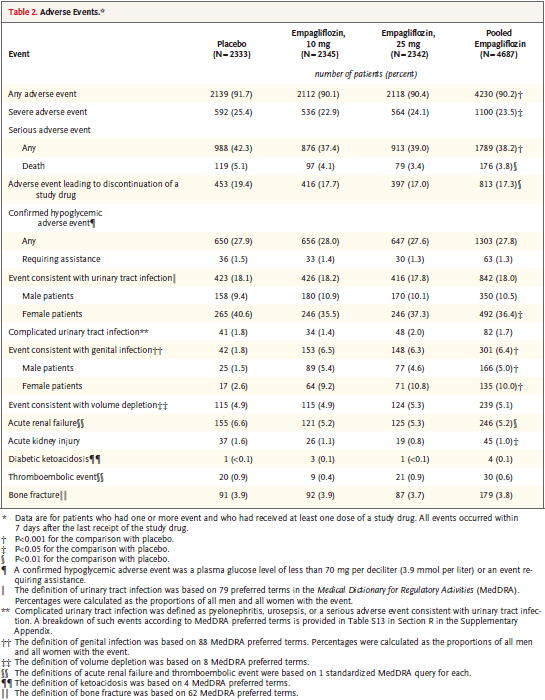
副作用の結果は,Table 2にある.低血糖はplacebo群で27.9%,empagliflozin群で27.8%と差がなかった.
ディスカッション:
本研究は,経口血糖降下薬においてメトホルミン,ピオグリタゾンに続く,心血管イベント抑制を証明したRCTである.しかも,ピオグリタゾンの効果を検証したPROactive では,primary outcomeで有意差が出なかったために無理やり有意差が出る複合アウトカムを「main secondary endpoint」として作り出したselective
outcome reporting(研究計画時に設定していないアウトカムを報告するバイアス)が問題となった.このため,経口血糖降下薬で心血管イベントを抑制するのは,メトホルミンのみとされてきた(DPP-4阻害薬も,単独のRCTでは心血管イベント抑制効果を証明できていない).
本研究ではprimary outcomeが有意に減ったが,その内訳では,心血管死は有意に減ったものの,心筋梗塞と脳卒中は減らなかった.したがって,心血管死のみを減らすと考えるべきだが,心筋梗塞と脳卒中が減らないのに,心血管死が減るというのは奇異 である.
他のアウトカムを見ると,心不全による入院が大きく減っているので,これが影響している可能性がある.
全死亡,心血管死が減ったのはなぜか
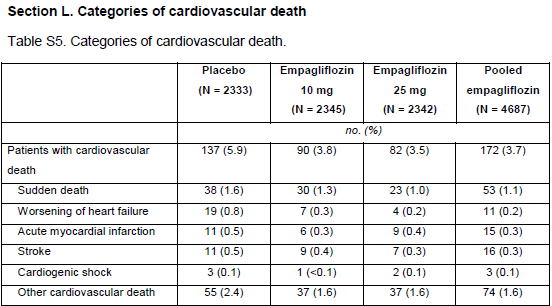
Table S5に心血管死の原因が示されている.これを見ると,決して心不全の増悪を減らせたことが心血管死減少の主因ではない ことが分かる.
「他の心血管死亡」とされているものが大きく占めているが,これが何者かは不明である.
ひょっとしたらTable 1のstrokeの発症率と下のTable S5のstrokeの発症率が異なる理由がわからずに困っている人がいるかもしれない.前者は純粋なstrokeの発症率,後者は心血管死の原因としてのstrokeの発症率である.したがって,後者のほうが少なくなるのは当然である.
副作用から見た本研究の妥当性
承認時の臨床試験の結果から,尿路感染症のリスクが上がることが分かっているが,本研究では,尿路感染症の発症率には群間の違いがなかった.
尿路感染症の発症リスクが上がらなかった代わりに性器感染症の発症リスクが上昇した.その原因は不明である.
RCT一般に言えることであるが,RCTでの症例数では検出力が不十分なため,安全性を証明することは極めて困難である.
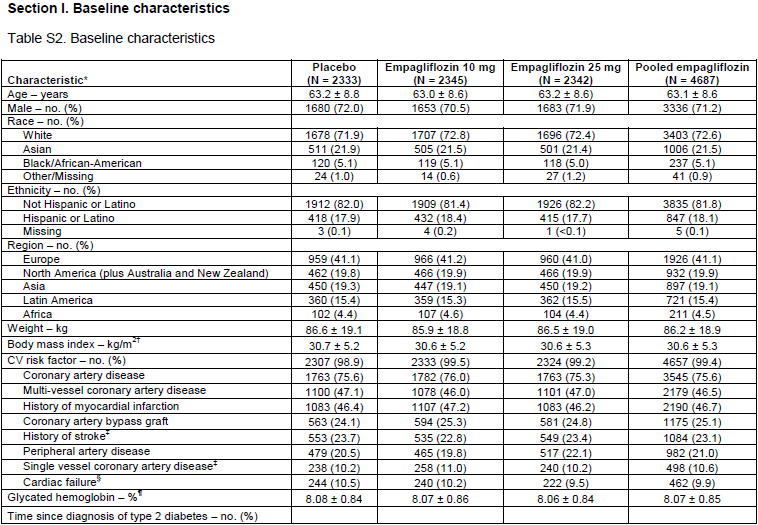
Baselineの特徴を検証する
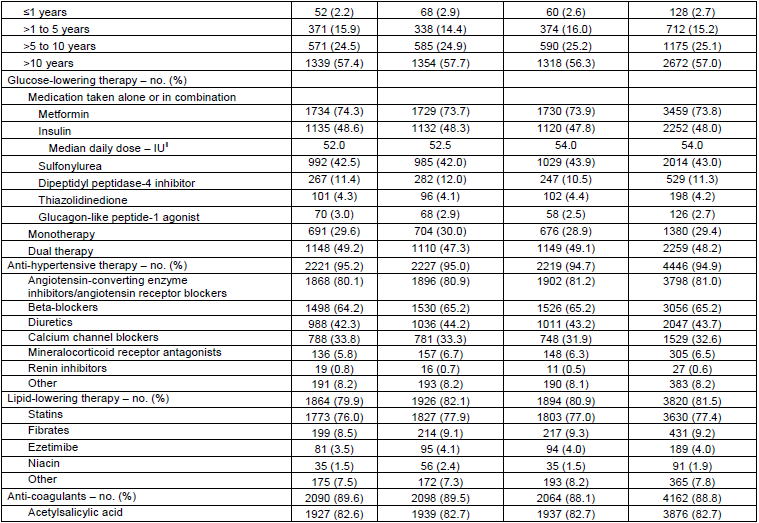
糖尿病罹病期間が10年以上がplacebo群で57.4%,empagliflozin群で57.0%と半数以上 だった.サブグループ解析では,罹病期間の違いによる効果の違いは検討されていなかった.
HbA1cは8.0%程度.
BMIは30程度と日本人の平均よりはやや肥満の集団.
約3/4の患者が冠動脈疾患に罹患している.多枝病変,心筋梗塞の既往のある患者が約半数,冠動脈バイパス術を受けた患者と脳卒中の既往のある患者が1/4と,かなり動脈硬化が進んで合併症を持っている患者が多い集団 である.
糖尿病治療薬は,3/4の患者でメトホルミン使用,半数の患者でインスリンを使用しているが,その1日単位数の中央値が52単位とかなり多い.SU剤は4割,DPP-4阻害薬が1割だった.単剤使用が3割,2剤併用が約半数 だった.
降圧剤は95%の患者で使われており,ACE阻害薬/ARBが8割,β遮断薬が6割,カルシウム拮抗薬は1/3の患者で使われていた.
脂質低下療法は8割で行われており,大部分はスタチンだった.
抗血小板薬・抗凝固薬は9割で使用されており,その大部分がアスピリン,クロピドグレルは1割,ワーファリンは6%だった.
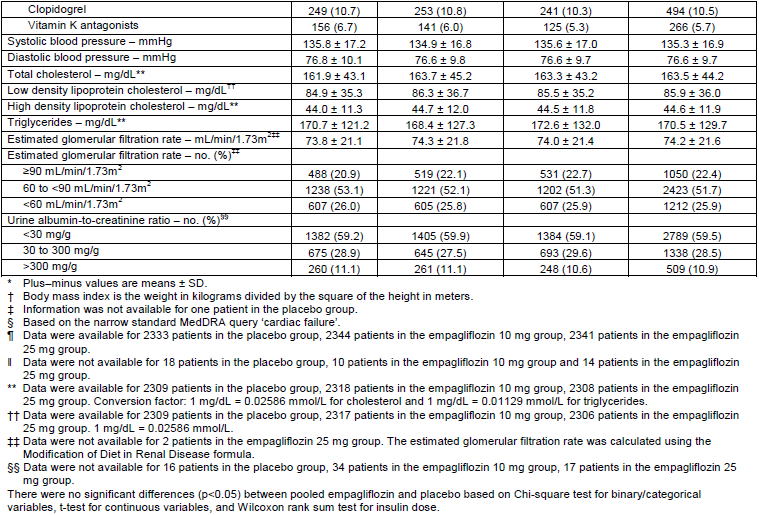
血圧は135/75mmHg程度,LDLコレステロールは85mg/dL,eGFRは70mL/min/1.73m2 台だった.
以上から,かなり動脈硬化が進んで合併症を多く持ち,他の治療がしっかり行われている患者を対象として行った研究であることが分かる.
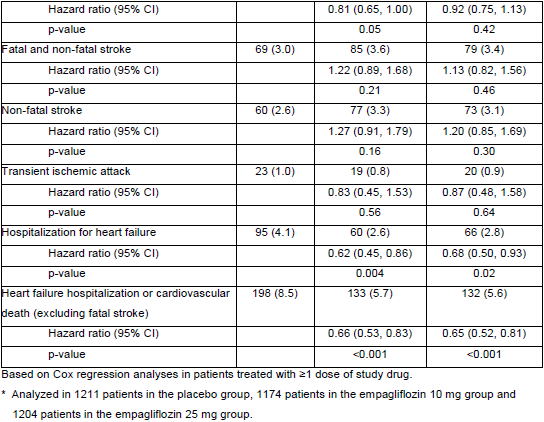
SGLT-2阻害薬empazliflozinはどれくらいの量使えばいいか
Table S6にempazliflozin 10mgと25mgの効果を比較した表がある.これを見ると,例えばprimary outcome は10mgではHR 0.85,25mgではHR 0.86とほぼ同じ効果推定値である.他の全てのアウトカムでも効果推定値が変わらない.つまり,10mgでも25mgでも効果はほぼ同等と考えられ,この研究ではempazliflozinに用量依存性の効果はない と思われる.
なお,empazliflozin全体では primary outcome に有意差があったにもかかわらず,10mgと25mgのそれぞれでは有意差が出ていないが,これは症例数が少なくなったために検出力が落ちたためと考えられる.10mgと25mgの効果推定値に違いがある場合は,両者を統合した結果の評価は慎重にするべきであるが,この研究結果としては,効果があるという結論に変わりはない.
副作用の起こり方に10mgと25mgの間に違いはないようだが,効果は同等である以上,empazliflozinを使用する場合は10mg使用すれば十分であり,効果不十分の場合でも25mgに増量することは意味が無いと考えられる.
結局のところ,どうすればいいのか:
本研究は,心血管合併症を有する2型糖尿病患者におけるSGLT-2阻害薬の全死亡,心血管死抑制効果を証明した最初のRCTであるとされる.
本研究に参加した患者は心血管合併症を有する2型糖尿病患者であり,本研究はそういった患者にすでにメトホルミンなどの他の経口血糖降下薬,ACE阻害薬などの降圧薬,スタチンなどの治療が行われているところに上乗せした効果を見たものである.
本研究の結果をもって,2型糖尿病患者における経口血糖降下薬を用いた治療の第一選択として本剤を代表とするSGLT-2阻害薬を用いるのは不適切である.あくまで,すでに心血管合併症を有する患者に対して,メトホルミンを使用してもHbA1c
8.0%以上の場合に,第2選択薬,第3選択薬として追加として使用することを考慮する薬剤であることに留意するべきである.また,仮にメトホルミンと同様に心血管イベントや死亡を減らす効果があるとしても,薬価差が大きいので,やはりメトホルミンが使える患者でSGLT-2阻害薬が第一選択になることはない.
Empazliflozinを使用する場合は10mg使用すれば十分であり,血糖降下作用が不十分であっても増量することに意味は無い.
1本のRCTで有効性が証明されただけで,積極的な処方を行うのは危険である.臨床試験は偶然効果があるという結果が出ることも多いので,今後の研究で真の効果が明らかになっていくまでは慎重を期するべきである.
本研究はプラセボ比較の非劣性試験であるので,優越性の検定はあくまで二次解析である.非劣性が証明されたついでにたまたま95%信頼区間が1をまたがなかったので,プラセボより有効だとしている.しかし,primary
outcomeに対する解析で非劣性と優越性の両方を検定するのであれば,ボンフェローに補正を行って有意水準は0.025とするべきである.また,非劣性マージンとしてHR 1.3を設定しているのだから,優越性を言うならば,優越性マージンも設定する必要がある.例えばHR 0.7を下回る必要があるはずで,HR
0.86(0.74〜0.99)では,プラセボとの「同等性」しか証明できていない のである(この場合,優越性マージンを30%とするのが妥当かどうかは議論が必要である).優越性を証明するためには,改めて優越性を一次解析としたランダム化比較試験を行う必要がある.
コメント:
※上記内容について,ご意見のある方は,是非こちら までお寄せ下さい.ご了解が得られれば,ご意見をコメント欄に掲載させていただきます(匿名可).ご連絡 をお願いいたします.
Copyrights(c)2004- Eishu NANGO