�@�z�[���@���@�Ȃ낭�@��
�Ȃ낭�|�����ُ��
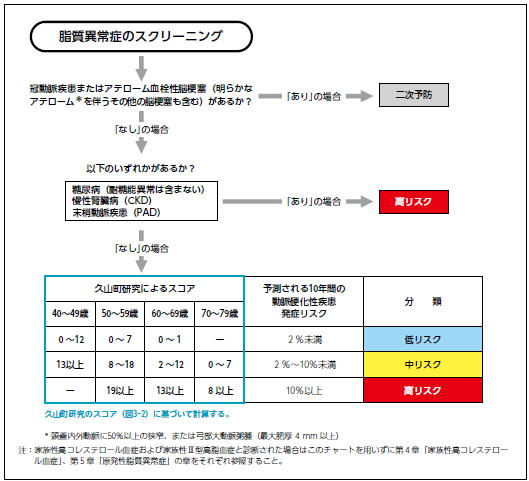
�@�f�f�E���X�N�]��
 ���C�N�Ɏ����ُ�ǂ̃X�N���[�j���O������ׂ����@�i���ڐV��2016/3/15�j ���C�N�Ɏ����ُ�ǂ̃X�N���[�j���O������ׂ����@�i���ڐV��2016/3/15�j
���N�f�f�œ�����O�̂悤�ɑ��肳��Ă��鎉���ُ�ǂł����C�X�N���[�j���O�̖ړI�͍ŏI�I�ȐS�؍[�ǂ̗\�h�Ƃ��C���S���ቺ�ł���͂��ł��D�Ƃ��낪�C�X�N���[�j���O�ɂ���Ď����ُ�ǂ��E���グ�Ď��Â��āC���ꂪ�����������ړI��B���ł��邩�ǂ����͊m���߂Ă݂�܂ł킩��܂���D�����ُ�ǂɑ���X�N���[�j���O�̖ړI���u�����Ɏ����ُ�ǂɑ��鎡�É�������邱�Ƃ������d�������������炵�C�����\������P����Ɗ��҂ł��閳�Ǐ�̊��ҌQ�����邱�Ɓv�ł���Ȃ�C���̑Ώۂƕ��@���͂�����Ƃ�����K�v������܂��D
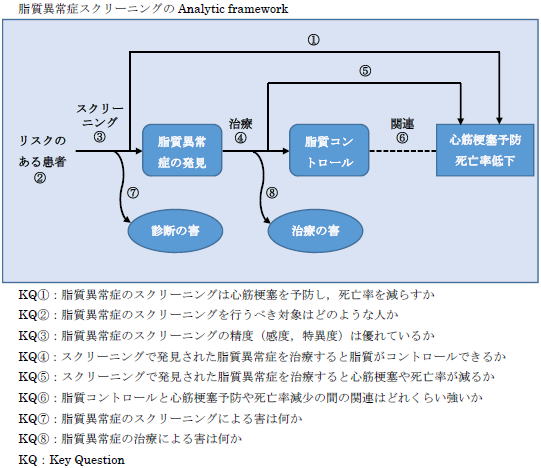
�f�ÃK�C�h���C���ɂ����ăX�N���[�j���O�̐��������ۂɂ́C�܂�analytic framework�ƌĂ����̂��쐬���܂��D����́C�������s�ׂ̐��������ۂɁC�ǂ̂悤�ȋ^�₪���炩�ɂȂ���ꂪ�\�ɂȂ邩�͂������̂ł��i���}�j�D�Ⴆ�X�N���[�j���O�̏ꍇ�C�P�Ɍ����@�̊��x�E���ٓx���D��Ă���Ƃ��������ł͂��̌�������낤�Ƃ������Ƃɂ͂Ȃ�܂���D�����ُ�ǂ����Ď��Â����Ă��\������P�����邱�Ƃ��o���Ȃ��悤�ȃ��X�N�̒�߂���C�܂��͍������銳�ҌQ�ł́A�����ُ�ǂ��X�N���[�j���O����K�v���Ȃ��ƍl�����܂��B
�܂��C�X�N���[�j���O�͏E���グ�ł�����C��ʓI�Ɍ����������炷���߂Ɋ��x������������cut off�l��p���܂����C���̕��g���[�h�I�t�œ��ٓx�͉�����܂��D���ٓx��������Ƃ������Ƃ͋U�z���������邱�ƂɂȂ�܂�����C�ߏ�f�f�������܂��D���܂�ߏ�f�f�������Ȃ�ƁC���̂��߂ɗ]�v�Ȍ�����s�K�v�Ȏ��Â���l���o�Ă��܂�����C�R�X�g�������ނ��ƂɂȂ�܂��D
�ȏ�̂悤�ɁC�X�N���[�j���O���s���ׂ������l����ۂɂ́Canalytic framework�Ŋe�����̋^���key question�Ƃ����`�ŕ\���C�ŏI�I�ɒN�ɍs���Η\�オ���P���邩���������Ă������ƂɂȂ�܂��D
�e���̐f�ÃK�C�h���C���ɂ����鎉���X�N���[�j���O�̐���
���{�����d���w��̓����d�������\�h�K�C�h���C��2012�N�Łi�ȉ��CJAS 2012�j�C�č���USPSTF��2008�N�ɔ��\���������C�J�i�_��2013�N�ɔ��\���ꂽCCS(Canadian Cardiovascular Society)�̎����ُ�ǂɂ��Ă̐f�ÃK�C�h���C���C���B��ESC(European Society of Cardiology)/EAS(European Atherosclerosis Society)��2011�N�̐f�ÃK�C�h���C���C�p��NICE��2014�N�ɔ��\�����f�ÃK�C�h���C���ɂ��鎉���ُ�ǃX�N���[�j���O�̐������ȉ��ɂ܂Ƃ߂܂��D���\�C���ɂ���Đ������قȂ�̂��킩��܂��D
| �� |
�f�ÃK�C�h���C���� |
�������e |
| ���{ |
JAS 2012 |
�E�{���i�X�N���[�j���O�j�̑Ώۂɂ́C��ɓ����d���댯���q�Ɋւ��u�������K�v�v�Ƃ��ꂽ���f���҂��܂܂�邪�C�����������ȂǓ����d���������̊�����L����ꍇ�A���邢�͂��łɎ����ُ�ǁA���A�a�A�������Ȃǂ̎��Â�o�ߊώ@���Ă��銳�҂ɂ��Ă��A����I�ɖ{���ɏ]���X�N���[�j���O�������{�s���A���X�N�Ƃ��̊Ǘ��̍ĕ]�����o���I�ɍs���ׂ��ł���B |
| �č� |
USPSTF (2008) |
�E�j����35�ł̓��[�`���ł̃X�N���[�j���O��������������iGrade A�j
�E�����������̃��X�N�̂��鏗����45�ł̓X�N���[�j���O��������������iGrade A�j
�E�����������̃��X�N�̂���20�`35�Βj����20�`45�Ώ����ł̓X�N���[�j���O�𐄏�����iGrade B�j
�E�����������̃��X�N�̂Ȃ�20�`35�Βj����20�`45�Ώ����ł̓��[�`���ł̃X�N���[�j���O���ǂ����邩������t���Ȃ��iGrade C�j
�E�����ُ�ǂ̃X�N���[�j���O�����Ƃ��ẮC���R���X�e���[����HDL-C�����ɑ��肷�� |
| �J�i�_ |
CCS (2013) |
�j���ł�40�Έȏ�A�����ł�50�Έȏ�܂��͕o��̊��҂ɑ��Đ�������B�������������������X�N���q�������҂ɂ��Ă͔N��Ɍ��炸�������� |
| ���B |
ESC/EAS (2011) |
40�Έȏ�̒j����50�Έȏ�܂��͕o��̏������X�N���[�j���O�̃��C���Ƃ��Đݒ肳��Ă���A���A�a�ȂNJ����������̃��X�N���q������ꍇ��A��N���ǂ̊����������̉Ƒ�����L����ꍇ�Ȃǂɂ́A�N��Ɍ��炸�X�N���[�j���O���{�s���� |
| �p�� |
NICE (2014) |
�E�v���C�}���P�A�ɂ�����S���ǎ����̈ꎟ�\�h�ɂ́C40�`74�Ńn�C���X�N���҂��E���グ�邽�߂̕�I�헪���s���ׂ��ł���D
�E10�N�S���ǎ������X�N��10%�ł���C�����ȃ��X�N�]�����s���D
�E���łɊ��������������݂���ꍇ�ƉƑ������R���X�e���[�����NJ��҂ł́i���łɃn�C���X�N�Ȃ̂Łj���X�N�]���͍s��Ȃ��D |
�ŏ��ɂ��������ʂ�C�X�N���[�j���O�̑ΏۂƂȂ�̂́C��������Ď��Â����ꍇ�Ɏ��Â̗��v������i���v���Q��R�X�g������j�ꍇ�Ɍ���܂��D
�����ُ�ǃX�N���[�j���O�̑ΏہF
�E�X�N���[�j���O�̑Ώۂ́C���A�a���]�[����CKD���҂ƁC���A�a�ȊO�̓����d�����X�N���S�đ����Ă����i60�`75�̋i���j���ŁC���k��������180 mmHg�ȏ�j����
�E��x���肵�Ċ�͈͂ł���C���̃X�N���[�j���O�͌����Ƃ���5�N�ȏ��
|
 �����d���������\�h�K�C�h���C��2022�N���@�i�ŏI�X�V2022/12/4�j �����d���������\�h�K�C�h���C��2022�N���@�i�ŏI�X�V2022/12/4�j
�{�M�̎����ُ�ǂ̃K�C�h���C����2012�N�C2017�N�ɑ����āC�T�N�Ԃ�ɉ��肳��C�u�����d���������\�h�K�C�h���C��2022�N���v�i�������J�j�Ƃ��ĂQ�O�Q�Q�N�V���S���ɔ�������܂����D�R���X�e���[���̃R���g���[���ڕW�͈ȉ��̒ʂ�ɂȂ��Ă��܂��D
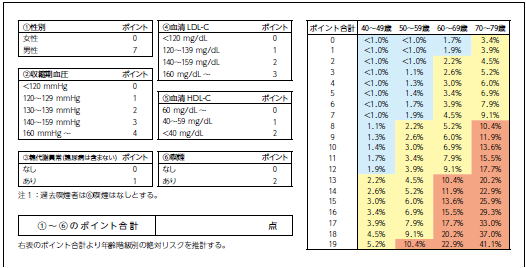
����͋v�R����������Z�o���ꂽ���X�N�\����p�����Ă���Ƃ����̂������ł��D
80�Έȏ�C40�Ζ����ł́C���̃t���[�`���[�g�ł̓R���g���[���ڕW�����߂��܂���D
 �����d���������\�h�K�C�h���C��2017�N���@�i�ŏI�X�V2017/12/11�j �����d���������\�h�K�C�h���C��2017�N���@�i�ŏI�X�V2017/12/11�j
�{�M�̎����ُ�ǂ̃K�C�h���C����2017�N�ɉ��肳��C�u�����d���������\�h�K�C�h���C��2017�N���v�i�������J����Ă��Ȃ��j�ł̃��X�N�]����NIPPON DATA���琁�c�X�R�A��p���邱�ƂɕύX����Ă��܂��D���̗��R�Ƃ��āC�ȉ��̂��̂��������Ă��܂��D
1�jLDL-C��HDL-C�̗�����\�����q�Ƃ��čl�����Ă���
2�jLDL-C�̃J�e�S�����ׂ����ݒ肳��Ă���
3�j�G���h�|�C���g�ɔ]�o�����܂܂�Ă��Ȃ�
4�j�A�E�g�J�������S�ł͂Ȃ��C�x���g���ǂƂ��Ă���
�u�����d���������\�h�K�C�h���C��2017�N�Łv���]�ڋ����̋K�����������CWebsite�ւ̓]�ڂ͉{���Ґ�����������Ă��Ȃ��ꍇ�ɂ�100���~�i�ŕʁj�ɂ��y�ԋ��������x����Ȃ���Ȃ炸�C�����ʼn^�c���Ă���{�E�F�u�T�C�g�ɓ]�ڂ��邱�Ƃ͕����I�ɕs�\�ł��D�L�����y������Ƃ����{���̐f�ÃK�C�h���C���̗��O�ɔ�����̂ŋK���ύX���Ă��炢�����ł����C���ۂɂ͂��̐��c�X�R�A�̓X�R�A�����O�����G�ŁC�����ɓ]�ڂ��Ă����p�I�ł͂���܂���D�u�����d���������\�h�K�C�h���C��2017�N�Łv�ł́C�u�������������Ǘ\���A�v��Web�Łv��z�z���Ă���C������͖����ł��̂ŁC���p����Ɨǂ��Ǝv���܂��D
 �����d���������\�h�K�C�h���C��2012�N���@�i�ŏI�X�V2013/1/7�j �����d���������\�h�K�C�h���C��2012�N���@�i�ŏI�X�V2013/1/7�j
�{�M�̎����ُ�ǂ̃K�C�h���C����2012�N�ɉ��肳��C�u�����d���������\�h�K�C�h���C��2012�N���v�i�������J����Ă��Ȃ��j�ł̃R���X�e���[���̃R���g���[���ڕW�͈ȉ��̒ʂ�ɂȂ��Ă��܂��D
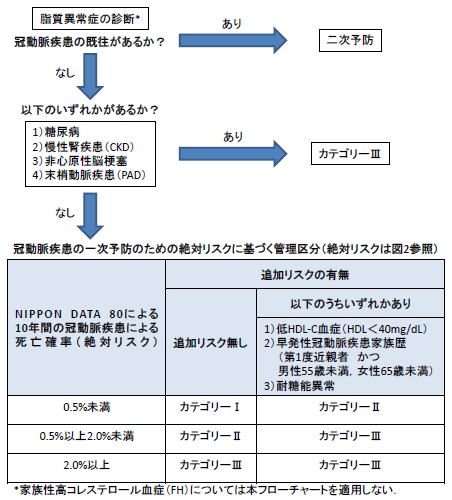
�}1�DLDL�R���X�e���[���Ǘ��ڕW�ݒ�̂��߂̃t���[�`���[�g
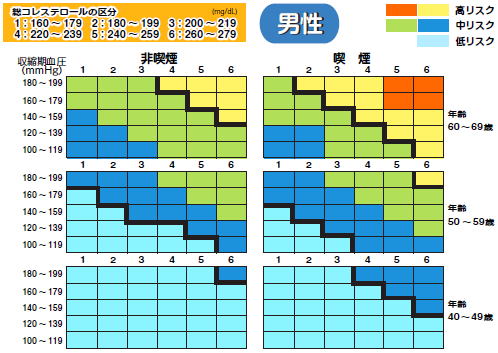
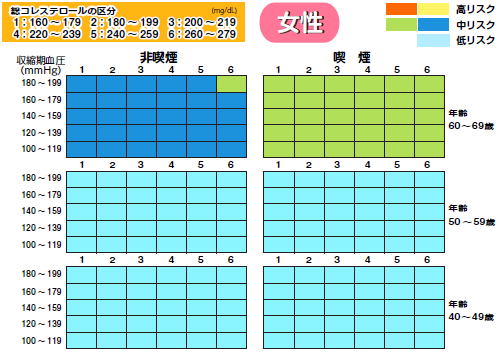
�}2�D���������S����X�N�]���`���[�g�i�ꎟ�\�h�j
�����X�N�� 5% �ȏ�10% ���� �� 2% �ȏ� 5% ����
�����X�N�� 1% �ȏ�2% ���� �� 0.5% �ȏ�1% ����
��X�N�� 0.5% ����
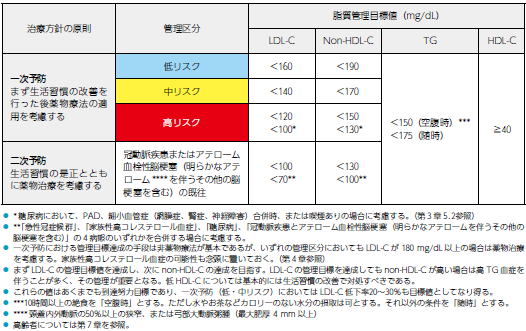
�\�D���X�N�敪�ʎ����Ǘ��ڕW�l
| ���Õ��j�̌��� |
�Ǘ��敪 |
�����Ǘ��ڕW�l�img/dL�j |
| LDL-C |
HDL-C |
TG |
non HDL-C |
�ꎟ�\�h
�܂������K���̉��P��
�s������C�Ö@��
�K�p���l������ |
�J�e�S���[�T
|
��160 |
��40 |
��150 |
��190 |
| �J�e�S���[�U |
��140 |
��170 |
| �J�e�S���[�V |
��120 |
��150 |
�\�h
�����K���̐����ƂƂ�
�ɖ��Â��l������ |
�����������̊��� |
��100 |
��130 |
�E�Ƒ������R���X�e���[�����ǂɂ��Ă�9�͂��Q�Ƃ̂��ƁD
�E����ҁi75�Έȏ�j�ɂ��Ă�15�͂��Q�Ƃ̂���
�E��N�҂ȂǂŐ���X�N���Ⴂ�ꍇ�͑����X�N�`���[�g�����p���C�����K���̉��P�̓��@�Â����s���Ɠ����ɐ���X�N�̐��ڂ𒍈Ӑ[���ώ@����D
�E�����̒l�͂����܂ł����B�w�͖ڕW�l�ł���D
�ELDL-C��20�`30%�̒ቺ��ڕW�Ƃ��邱�Ƃ��l������D
�Enon HDL-C�̊Ǘ��ڕW�́C��TG�����̏ꍇ��LDL-C�̊Ǘ��ڕW��B��������̓ڕW�ł���DTG��400mg/dL�ȏエ��ѐH��̌��̏ꍇ�́Cnon
HDL-C��p����D
�E������̃J�e�S���[�ɂ����Ă��Ǘ��ڕW�B���̊�{�͂����܂ł������K���̉��P�ł���D
�E�J�e�S���[�T�ɂ�����Ö@�̓K�p���l������LDL-C�̊��180mg/dL�ȏ�Ƃ���D
�i���{�����d���w��i�ҁj�F�����d���������\�h�K�C�h���C��2012�N�ŁC���{�����d���w��C2012�j
|
�ȏ�̂悤�ɁC���X�N�]����2007�N�łƈقȂ��đ�ϔώG�ɂȂ��Ă��܂��D�������C�d�v�Ȃ��Ƃ́C���ꂪNIPPON DATA 80�Ƃ����u�w�f�[�^�i�ώ@�����j�����ɍ���Ă��邱���ł���C����X�N�̐�����s���悤�ɑ����Ă��邱�Ƃ͕]���ł��܂����C����X�N�������l������Ƃ����ċ��͂�LDL-C���������玀�S���X�N�����点�邩�ǂ����͕ʖ��ł��D�i����قǍׂ����j����X�N�ʂɃR���X�e���[�������������x�i�Ǘ��ڕW��ς������Ɓj�ɂ���Ăǂ̂悤�Ȍ��ʂ�������̂��ɂ��ẮC�ߋ��̗Տ������ł��قƂ�ǖ��炩�ɂ���Ă��܂���D���̂��߂��C���̃K�C�h���C���ł��C�u�����i�Ǘ��ڕW�j�̒l�͂����܂ł����B�w�͖ڕW�l�ł���v��C�uLDL-C��20�`30%�̒ቺ��ڕW�Ƃ��邱�Ƃ��l������v�ȂǂƎ���̈����L�q�ɂȂ��Ă��܂��D
�܂��CNIPPON DATA 80�ł�10�N�Ԃ̊����������ɂ�鎀�S�m����������Ă���̂ł����āC�����S�⊥�����������Ǘ��C�]�������Ǘ��͍l������Ă��Ȃ����Ƃɂ����ӂ���ׂ��ł��iNIPPON DATA 80�ɂ��10�N�Ԃ̐S�����ɂ�鎀�S���X�N�̎Z�o�c�[����web�Ō��J����Ă��܂��j�D
����1�C���̃t���[�`���[�g�ł́C40�`69�̊��҂�����ΏۂƂ��Ă��܂��D�u����ҁi75�Έȏ�j�ɂ��Ă�15�͂��Q�Ƃ̂��Ɓv�Ə�����Ă��܂����C70�`75�ł����̃t���[�`���[�g�ł̓R���g���[���ڕW�����߂��܂���D
���̃t���[�`���[�g��p���ăR���g���[���ڕW�����߂�ۂɂ́C�����������_�ɒ��ӂ���K�v������܂��D
���ŐV�̐f�ÃK�C�h���C���ł́C���X�N�]���̂��߂ɂ͐��c�X�R�A���p�����Ă��܂��D���c�X�R�A�ɂ��Ă͈ȉ������Q�ƁD
 �S���ǃ��X�N�]���@�i���ڐV��2016/3/15�j �S���ǃ��X�N�]���@�i���ڐV��2016/3/15�j
�e���̐f�ÃK�C�h���C���ł́C���ꂼ�ꎩ���̐S���ǃ��X�N�]���c�[����p���Ă��܂��D
�ȉ��ɓ��ĉp�̃��X�N�]���c�[�����Љ�܂��D
���X�N�]���ɂ́C�����̃c�[����p����̂������ł��D
�@����
 �����̏ꍇ�C�����������ꎟ�\�h�ɂ͎����ُ�ǎ��Ö�̓K���͂Ȃ��@�i���ڐV��2016/3/15�j �����̏ꍇ�C�����������ꎟ�\�h�ɂ͎����ُ�ǎ��Ö�̓K���͂Ȃ��@�i���ڐV��2016/3/15�j
���f�Ŏ����ُ���w�E����銳�҂͌��₽���C�o�㒆�N�����Ɍ����Ă����̐��͑�ϑ����ł��D�������������҂͎��Â�����ׂ��ł��傤���D
�����������̊����̂��銳�҂ł̓X�^�`���͕K�{��ł����C�����������̊����̂Ȃ����҂ł͓����悤�ɂ͂����Ȃ��悤�ł��D
���{�����d���w��́u�����d���������\�h�K�C�h���C��2012�N���v�i�������J����Ă��Ȃ��j�ɂ���NIPPON DATA 80�ɂ�郊�X�N�]���Ŏ��ÑΏۂ����߂�͈̂ꌩ���[�Y�i�u���ȕ��@�ł����C����NIPPON DATA 80�̃��X�N�`���[�g�ƏƂ炵���킹�Ď��Â̓K�ۂ����߂�͔̂ώG�ł��D�����Ɗo���₷�����@�͂Ȃ��̂ł��傤���D
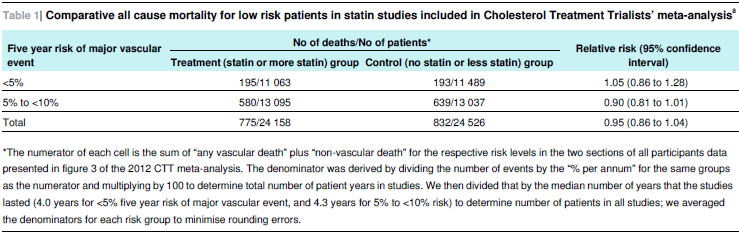
��X�N���҂ɑ���X�^�`�����Â̌��ʂ�������Cholesterol Treatment Trialists'(CTT)�̃��^�A�i���V�X�iLancet 2012;380:581�CBMJ 2013;347:f6123�j�ɂ��C5�N�Ԃ̎�v���ǃC�x���g�imajor vascular events: MVE�j�̃��X�N��10%�����ł͎��S����RR 0.90�i0.81�`1.01�j�ƗL�ӂɂ͌��炸�C5%�����ł�RR 1.05�i0.86�`1.28�j�Ƌt�ɑ�����\�����炠��܂����D�ꎟ�\�h�ł����Ă��C���X�N�ɂ���Ď��Ì��ʂ͕ς���Ă���̂ł��D
�����Ŏ�v���ǃC�x���g�iMVE�j�ƌĂ�ł�����̂ɂ́C��v�������C�x���g�i��v���I�S�؍[�ǂ܂��͊��������S�j�Ɣ]�����Ɗ����ǍČ��p���܂�ł��܂��D
�Ƃ���ŁCNIPPON DATA 80�ɂ�郊�X�N�]���ŁC���{�����d���w��́u�����d���������\�h�K�C�h���C��2012�N���v�ł́C���������S�̐���X�N���ō��ł�10�N�Ԃ�10%�����ƂȂ��Ă��܂��D�J�e�S���[�̓J�e�S���[�T�i0.5% �����j�C�J�e�S���[�U�i0.5% �ȏ� 2.0% �����j�C�J�e�S���[�V�i2.0% �ȏ�j��3�ɕ�����Ă��܂��D
�����ŁC�J�e�S���[�V�ł���u10�N�Ԃ̊����������ɂ�鎀�S�m����2.0% �ȏ�v�Ƃ����̂́C���MVE�ł͂ǂꂭ�炢�ɑ�������̂ł��傤���D���́C�c�O�Ȃ���NIPPON
DATA 80�ł�MVE���ǂꂭ�炢�N����̂��Ƃ����f�[�^�����\����Ă��܂���D
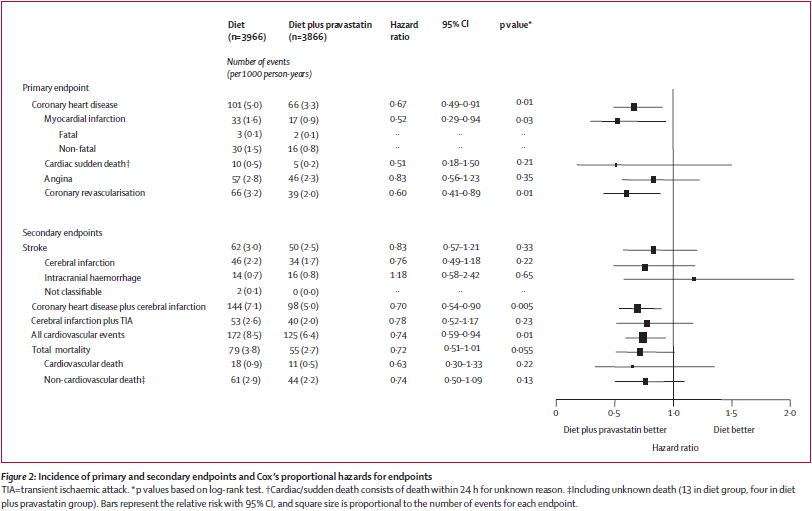
���������S���X�N�Ǝ�v���ǃC�x���g�iMVE�j���X�N�̑���
��`�����X�N�̓��{�l���҂ɂ����ĐH���Ö@��ΏƂƂ��ăv���o�X�^�`���̐S���ǃC�x���g�ꎟ�\�h���ʂ�������MEGA study�iLancet 2006;368:1155�j�ł́C5.3�N�Ԃ̊ώ@�ŐH���Ö@�P�ƌQ�̒v���I�S�؍[�ǁi�������������ɂ�鎀�S�j���i3/3966���j0.08%�Ȃ̂ɑ��CMVE���Ǘ����i(33+62+66)/3966���j4.69%�ł����D�������C�������ɂ�����ꎟ�\�h�ł����Ă��C5.3�N�ԂŒv���I�S�؍[�ǂ̔��ǂ�0.08%�Ƃ����̂͏��������܂��D����́C�C�x���g���ǐ������Ȃ����߁C���܂��ܐS�؍[�ǂŖS���Ȃ����l�����Ȃ������ƍl�����܂��D
����C�S���ǎ��S�́i18/3966���j0.45%�ł����C�S�؍[�LjȊO�̐S���ǎ����Ŏ��S���Ă���̂��S�؍[�ǂł̎��S��5�{�����邱�ƂɂȂ�܂��D����͂�����ƈ�a��������܂��D�����Ƃ����CMVE�ɂ͊����ǍČ��p���܂܂�܂����CMEGA
study�ł͂��̎{�s�Ⴊ�����ł�����C�^�̊����������͂����Ə��Ȃ��ƍl�����܂��D
�����ŁC�S���ǎ��S0.45%�ɑ���MVE 4.69%�ł��邱�Ƃ��l������ƁC
���������S2.0%�ɑ�������MVE��20%���x
�ɂȂ�܂��D�܂�C��̃��^�A�i���V�X�̌��ʂ̎����ʂ莀�S������Ȃ�MVE��5�N�Ԃ�10%�ł�����C10�N�Ԃ���20%�ɂȂ�C�ł����X�N�̍����J�e�S���[�V�ł��X�^�`�����Âɂ���Ď��S������Ȃ��ƌ����܂��D
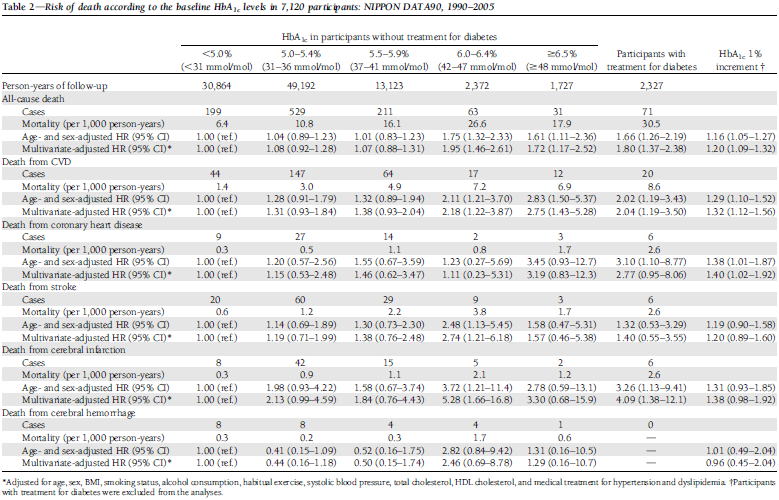
���A�a����
�ł́C�ꎟ�\�h�ł͂��ׂĂ̊��҂Ŏ����ُ�ǂ̖��Â��S���s�v�ł��傤���D
NIPPON DATA 90�iDiabetes Care 2013;36:3759�j�̃f�[�^����C���{�l���A�a���҂̊��������S����1000�l�N��2.6�C���Ȃ킿�P���v�Z��10�N�Ԃ̊����������ɂ�鎀�S�m����2.6%�ƍ������Ƃ�������Ă��܂��D������2006�N�̃V�X�e�}�e�B�b�N���r���[�iBMJ 2006;332:1115�j�ɂ����āC���A�a���҂�ΏۂƂ���6���̃��^�A�i���V�X�ɂ��C�������C�x���g�̈ꎟ�\�h��RR 0.79�i95%CI 0.7�`0.89�j�{�ɗL�ӂɌ������Ƃ�������Ă��܂��̂ŁC���A�a���҂ł͖��Â��s�����ق��������ł��傤�D
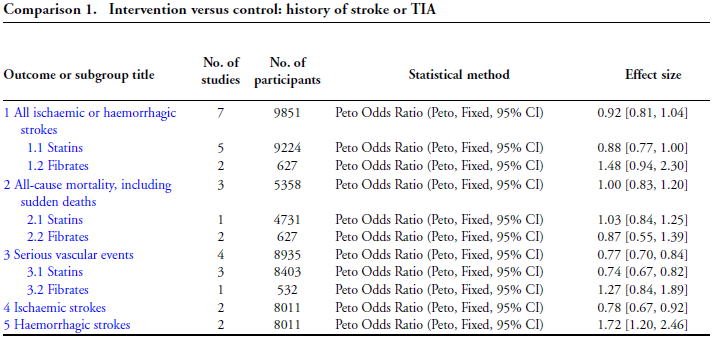
�]�[�ǂ̊����̂��銳��
�@�]�[�ǂ̊����̂��銳�҂��A�X�s������~���܂ƂƂ��ɃX�^�`�����g�p���邱�Ƃ̓����b�g������ł��傤���D
�@2009�N�ɔ��\���ꂽ�R�N�������r���[�ł́C7����RCT�̃��^�A�i���V�X�ŁC�]�[�ǂ�TIA�̊����̂��銳�҂̎����ُ�ǎ��Ö�g�p�͔]�[�ǂƔ]�o���̔��ǂ�OR
0.92�i0.81�`1.04�j�ƍĔ���L�ӂɌ��炷���Ƃ��ł��܂���ł����D�����C�t�B�u���[�g��OR 1.48�i0.94�`2.30�j�ƊQ�̌X��������C�X�^�`�������ł�5���̃��^�A�i���V�X��OR
0.88�i0.77�`1.00�j�Ɣ]�[�ǂ�]�o������⌸�炷�Ƃ������̂ł����D���̃R�N�������r���[�ł́C�����S�͌��点���C�]�[�ǂɌ����OR 0.78�i0.67�`0.92�j�ƗL�ӂɌ��点�܂������C�t�ɔ]�o����OR
1.72�i1.20�`2.46�j�ƗL�ӂɑ����錋�ʂł����D
�@���_�Ƃ��āC�]�[�ǂ̊����̂��銳�҂̓X�^�`���p���Ă������ł����C�o���̃��X�N�������邱�Ƃ�O���ɒu���Ȃ���C�Ⴆ�Δ]�o���̊����̂��銳�҂ł͎g�p���T����ȂǂƂ�������������������܂����D
CKD����
�@���͂����Ă��Ȃ�CKD���҂�ΏۂƂ���2014�N�̃R�N�������r���[�iCDSR 2014:CD007784�j�ł́C13����RCT�̃��^�A�i���V�X�ŁC�X�^�`�����Âɂ���v���ǃC�x���g��RR 0.72�i0.66�`0.79�j�C�����S��RR 0.79�i0.69�`0.91�j�C�S���ǎ��S��RR
0.77�i0.69�`0.87�j�Ƃ�������L�ӂɌ������܂����D
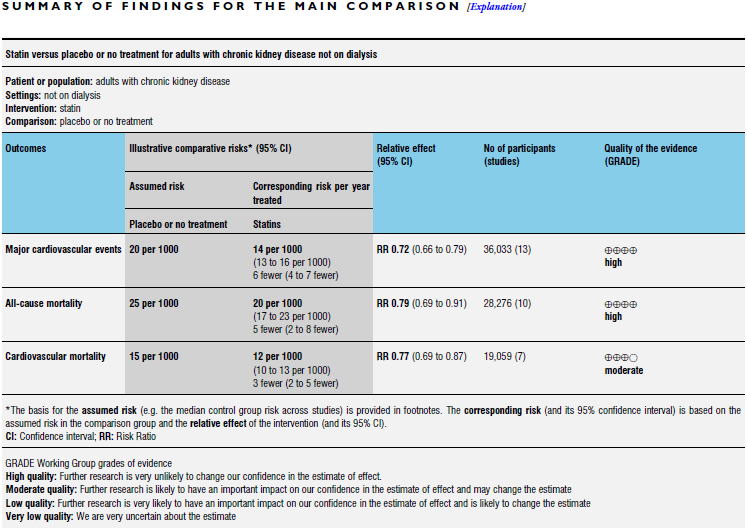
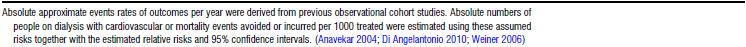
����ɑ��āC���͒���CKD���҂�ΏۂƂ���2013�N�̃R�N�������r���[�iCDSR 2013:CD004289�j�ł́C13����RCT�̃��^�A�i���V�X�ŁC�X�^�`�����Âɂ���v���ǃC�x���g��RR 0.95�i0.88�`1.03�j�C�����S��RR 0.96�i0.90�`1.02�j�C�S���ǎ��S��RR
0.94�i0.84�`1.06�j�Ƃ�������L�ӂȌ����͎����܂���ł����D
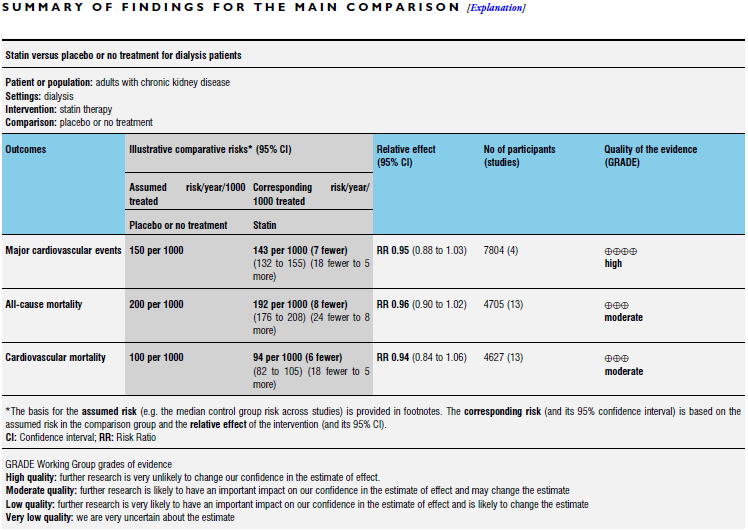

���_�Ƃ��ẮC�X�^�`�����g�p���邱�Ƃɂ�郁���b�g�͓��͒��łȂ�CKD���҂ł͂���܂����C���͒���CKD���҂ł͂���܂���D
���n�C���X�N����
�@�܂��CNIPPON DATA 80�̃��X�N�]����10�N�Ԃ̊����������ɂ�鎀�S�m����5�`10%�ƍ����Ȃ�60�`75�̋i���j���ŁC���k��������180 mmHg�ȏ�̏ꍇ�i�܂�C���A�a�ȊO�̃��X�N���S�đ����Ă���j���j���C���Â��s�����ق��������ł��傤�D
�@�����C������O�ȊO�̊��҂���̈ꎟ�\�h�ł����Â��s���Ă͂����Ȃ��Ƃ������Ƃł͂Ȃ��C��胊�X�N���������҂����C�ǂ����Ă��Ö@���s�������Ɗ�]���銳�҂���ɂ́C�ǂ̂悤�ȃA�E�g�J����ړI�Ɏ��Â��邩���m�F���C���Ì��ʂɂ��Ęb���������Ŏ��Â��J�n���邱�Ƃ�����܂��D
�����������ꎟ�\�h�ɑ���Ö@�̓K��
- �x�[�X���C�����X�N�i�x�[�X���C���̐S���ǃC�x���g���ǃ��X�N�j�̍l��������{�D���ÓK���͂��ׂăx�[�X���C�����X�N�̍����Ō��܂�
- ��{�I�ɁC�ꎟ�\�h�ł͋i���Ȃǂ̐����K�����P�𒆐S�ɐ����CLDL�R���X�e���[���̒l���ǂ�قǍ����Ă��C�����Ƃ��ĖÖ@�͍s��Ȃ��iLDL�R���X�e���[���l�����S���ǃ��X�N���厖�j
- ���A�a���҂ł�LDL�R���X�e���[�� 120 mg/dL�����ɂȂ�悤�Ɏ�������i�\�h�ƈقȂ�C���ÑO����LDL-C��120 mg/dL�ł���Ζ��Â͕s�v�j
- �]�[�ǁCCKD�����i�������C���͒��̊��҂������j�͎��Â��Ă��悢�i�ڕWLDL�R���X�e���[�� 120 mg/dL�j
- 60�`75�̋i���j���ŁC���k��������180 mmHg�ȏ�i�܂�C���A�a�ȊO�̓����d�����X�N���S�đ����Ă���j���j�̏ꍇ���C���Â��s��
|
 �X�^�`���̑I�ѕ��@�i���ڐV��2014/5/21�C�ŏI�X�V2022/12/4�j �X�^�`���̑I�ѕ��@�i���ڐV��2014/5/21�C�ŏI�X�V2022/12/4�j
���ݖ{�M�ŏ��F����Ă���X�^�`���͈ȉ��̒ʂ�ł��D��������܂����C�Ⴂ�͂قڗ͉��̈Ⴂ�i�ǂꂾ�����͂�LDL-C�������邩�j�����ƍl���ėǂ��Ǝv���܂��D
| ���� |
���i�� |
��ʖ� |
������ |
�� |
|
| �X�^���_�[�h�X�^�`�� |
���o���`�� |
�v���o�X�^�`�� |
���O���^�u���X�g���E�}�C���[�Y�X�N�C�u |
50.5�~/5mg�C94.8�~/10mg |
�㔭�i���� |
| ���{�p�X |
�V���o�X�^�`�� |
���L����^�����N |
112.4�~/5mg�C221.8�~/10mg�C447.8�~/20mg |
�㔭�i���� |
| ���[�R�[�� |
�t���o�X�^�`�� |
�m�o���e�B�X�t�@�[�}�^�c�ӎO�H���� |
38.9�~/10mg�C69�~/20mg�C99.1�~/30mg |
�㔭�i���� |
| �X�g�����O�X�^�`�� |
���s�g�[�� |
�A�g���o�X�^�`�� |
�A�X�e���X����^�t�@�C�U�[ |
65.5�~/5mg�C107.9mg/10mg |
�㔭�i���� |
| ���o�� |
�s�^�o�X�^�`�� |
���a�n�� |
63.2�~/1mg�C119.8�~/2mg |
�㔭�i���� |
�X�g�����O�X�^�`��
�i�X�[�p�[�X�^�`���j |
�N���X�g�[�� |
���X�o�X�^�`�� |
����`����^�A�X�g���[�l�J |
68.1�~/2.5mg�C131.5�~/5mg |
�㔭�i�Ȃ� |
���ꎟ�\�h�Ɠ\�h�ɂ����鎡�ÑO�l��LDL�R���X�e���[���ɉ������X�^�`���̑I�ѕ�
�ꎟ�\�h
���@�ōł��p�ɂ�LDL�R���X�e���[���̃R���g���[�����s���̂́C���A�a���]�[���̊��҂ł��D
�K���Ȃ��ƂɁC�������2007�N�ł̃K�C�h���C���ƕς�炸�C���A�a��CKD�CPAD�ɂ�����R���g���[���ڕW�́CLDL�R���X�e���[����120mg/dL�ł��D���A�a��PAD�����C���A�a�������Ǐ�Q�̍����C�܂��͋i������̏ꍇ�ɂ́CLDL�R���X�e���[����100 mg/dL���ڕW�ɂȂ�D�D
�����ُ�ǂ̎��Âōł��厖�Ȃ̂́CLDL�R���X�e���[���̃R���g���[���ł��D
HDL�R���X�e���[���͒��ڏ㏸������ǂ���܂��Ȃ��ł����C�������b�͂��̃R���g���[�����S���ǎ����̗\�h�ɗL���Ƃ���G�r�f���X���Ȃ�����ł��D
�\�h
�����������܂��͔]�����̊����̂���l���ΏۂƂȂ�D
�\�h�ł͑S��ɖÖ@���s���D
LDL-C�l�ɂ���ėp����X�^�`���̎�ނƗp�ʂ����肷��D
LDL-C 100 mg/dL�i70 mg/dL�j������ڕW�Ƃ���D
���ۂɎ��Â���ۊe�X�^�`���ɂ�����LDL-C�ቺ���ɂ��ẮC UpToDate�́uLipid lowering with statins�v�Ɋe�X�^�`���̗p�ʂ�LDL�R���X�e���[���ቺ���̊W�������\���ڂ��Ă��܂��D
����́C�e�X�^�`���̌��ʂ�����̂ɂƂĂ��֗��ł��D
LDL�R���X�e���[���ቺ���̃f�[�^����t�Z�����C���ÑO�l��LDL�R���X�e���[���ɉ������I�����ׂ��X�^�`�����ȉ��̕\�ɂ܂Ƃ߂܂��D
�������C�H���Ö@�̌��ʂ����҂ł���Ƃ��ɂ́C��������������Ė�܂̑I������Ɨǂ��ł��傤�D
�ꎟ�\�h�Ŏ��Â���ꍇ�iDM�CCKD�CPAD���ҁC�����X�N����
�ڕWLDL-C��120mg/dL�j
LDL�R���X�e���[��
���ÑO�l |
�ڕW�ቺ�� |
�I�Ԃׂ��X�^�`�� |
�� |
| 265 mg/dL |
�|55% |
���X�o�X�^�`��20 mg* |
52.4�~
|
| 240 mg/dL |
�|50% |
���X�o�X�^�`��10 mg* |
26.2�~ |
| 220 mg/dL |
�|45% |
���X�o�X�^�`��5 mg |
13�~ |
| 200 mg/dL |
�|40% |
�A�g���o�X�^�`��10 mg
���X�o�X�^�`��2.5 mg |
20.7�~
8.6�~ |
| 185 mg/dL |
�|35% |
�A�g���o�X�^�`��5 mg |
10.1�~ |
| 150 mg/dL |
�|20% |
�v���o�X�^�`��10 mg |
13.7�~ |
| 130 mg/dL |
�|10% |
�v���o�X�^�`��5 mg |
10.1�~ |
| ��120 mg/dL |
0% |
���Â̕K�v�Ȃ� |
|
|
|
�ꎟ�\�h�Ŏ��Â���ꍇ�iDM��PAD�C�����Ǐ�Q�����C
�i������̏ꍇ�C�ڕWLDL-C��100mg/dL�j
LDL�R���X�e���[��
���ÑO�l |
�ڕW�ቺ�� |
�I�Ԃׂ��X�^�`�� |
�� |
| 220 mg/dL |
�|55% |
���X�o�X�^�`��20 mg* |
52.4�~
|
| 200 mg/dL |
�|50% |
���X�o�X�^�`��10 mg* |
26.2�~ |
| 180 mg/dL |
�|45% |
���X�o�X�^�`��5 mg |
13�~ |
| 170 mg/dL |
�|40% |
�A�g���o�X�^�`��10 mg
���X�o�X�^�`��2.5 mg |
20.7�~
8.6�~ |
| 155 mg/dL |
�|35% |
�A�g���o�X�^�`��5 mg |
10.1�~ |
| 125 mg/dL |
�|20% |
�v���o�X�^�`��10 mg |
13.7�~ |
| 110 mg/dL |
�|10% |
�v���o�X�^�`��5 mg |
10.1�~ |
| ��100 mg/dL |
0% |
���Â̕K�v�Ȃ� |
|
|
�\�h�Ŏ��Â���ꍇ�i�ڕWLDL-C��100mg/dL�j
LDL�R���X�e���[��
���ÑO�l |
�ڕW�ቺ�� |
�I�Ԃׂ��X�^�`�� |
LDL-C
����\���l |
| 220 mg/dL |
�|55% |
���X�o�X�^�`��20 mg* |
100 mg/dL |
| 200 mg/dL |
�|50% |
���X�o�X�^�`��10 mg* |
| 180 mg/dL |
�|45% |
���X�o�X�^�`��5 mg |
| 170 mg/dL |
�|40% |
�A�g���o�X�^�`��10 mg
���X�o�X�^�`��2.5 mg |
| 155 mg/dL |
�|35% |
�A�g���o�X�^�`��5 mg |
| 140 mg/dL |
�|30% |
90 mg/dL |
| 120 mg/dL |
�|15% |
80 mg/dL |
| 100 mg/dL |
�}0% |
65 mg/dL |
| 80 mg/dL |
�| |
50 mg/dL |
| 60 mg/dL |
�| |
40 mg/dL |
�ŏ�����ڕW�ɒB���Ă��Ă��Œ���A�g���o�X�^�`��5 mg���g�p���� |
|
�\�h�Ŏ��Â���ꍇ�i�ڕWLDL-C��70mg/dL�j
LDL�R���X�e���[��
���ÑO�l |
�ڕW�ቺ�� |
�I�Ԃׂ��X�^�`�� |
LDL-C
����\���l |
| 155 mg/dL |
�|55% |
���X�o�X�^�`��20 mg* |
70 mg/dL |
| 140 mg/dL |
�|50% |
���X�o�X�^�`��10 mg* |
| 125 mg/dL |
�|45% |
���X�o�X�^�`��5 mg |
| 115 mg/dL |
�|40% |
�A�g���o�X�^�`��10 mg
���X�o�X�^�`��2.5 mg |
| 105 mg/dL |
�|35% |
�A�g���o�X�^�`��5 mg |
| 100 mg/dL |
�|30% |
65 mg/dL |
| 80 mg/dL |
�|12.5% |
50 mg/dL |
| 70 mg/dL |
�}0% |
45 mg/dL |
| 60 mg/dL |
�| |
40 mg/dL |
| 50 mg/dL |
�| |
32.5 mg/dL |
�ŏ�����ڕW�ɒB���Ă��Ă��Œ���A�g���o�X�^�`��5 mg���g�p���� |
*�Y�t������̋L�ڂ���C���X�o�X�^�`����5mg�ȉ�����J�n���Ȃ���Ȃ�܂���D
���Ȃ݂ɁC�X�^�`���͋����ɂ���āCstrong statin�Ƃ��Csuper statin�Ƃ����������������܂����C�P�ɗ͉��̖�肾�Ǝv���܂��D
�܂�C�����ɔ������ꂽ�Â�statin�ł��C�ʂ𑝂₹��LDL�͉�����Ƃ������Ƃł��D
����́C�V������܂����F����Ƃ��ɂ́C���ɂ����܂��D��Ă��邱�Ƃ��ؖ����Ȃ��Ƃ����Ȃ��̂ŁC���LDL�̉�����͉���ݒ肷��K�v������Ƃ���������邽�߂ł��D
�X�^�`���ɂ�鉡��ؗZ����
����ؗZ���ǂ͔��Ǘ���100,000�l�N������3.4�l�Ə��Ȃ��ł����C���ǂ�����v������10%�ƕ|������p�ł��D
�X�^�`���̋����������Ȃ�قǁC����ؗZ���ǂ̔��Ǘ��͍����Ȃ��Ƃ���Ă��܂��̂ŁC�K�v�ȏ�ɒቺ���̍������I�Ԃ͔̂����������ǂ��ł��傤�D
�ł�LDL�R���X�e���[�������͂ɉ����郍�X�o�X�^�`���́C�t��Q��75�{���ǂ��C���F�O�̗Տ������ʼn���ؗZ���ǂ����ǂ��܂����D
���������āC�R���X�e���[���̎��Â̂��߂ɂ́C�K�v�Œ���i�R���g���[���ڕW��B����������Ǝア�j�̖�܂�p����ׂ��ł��D
�ʏ���X�^�`���J�n���琔�T�ԁ`�������ȓ��ɋN����܂��D
����ؗZ���ǂ܂ł����Ȃ��Ă��ؓ��ɂ�E�͂ȂNj؏ǏN���邱�Ƃ�����܂��D2�`11%�ƕp�ɂɋN����Ƃ���Ă��܂��D
����CK�͏㏸���Ȃ����Ƃ�����܂��D
���ǂ���Ƃ��ɂ͐����̌o�߂ŋN����C�X�^�`���𒆎~����ΐ����`���T�Ԃʼn��܂��D���������āC����ؗZ���ǂ𑁊���������ړI���O���̂��тɃX�^�`�����p���҂Ƀ��[�`���Ō���CK�����j�^�����O���邱�Ƃ͈Ӗ����Ȃ��Ƃ���Ă��܂��D
 �X�^�`���͓��A�a�𑝂₷�@�i�ŏI�X�V2010/3/3�j �X�^�`���͓��A�a�𑝂₷�@�i�ŏI�X�V2010/3/3�j
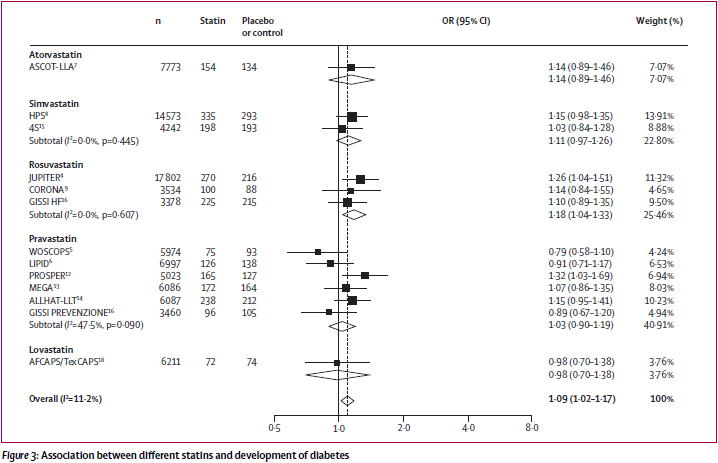
�X�^�`���̗͉����オ��Ό��ʂ��傫�����Q�������Ƃ����̂́C2010�N3��2�����s��Lancet�Ɍf�ڂ��ꂽ���^�A�i���V�X�iLancet 2010;375:735�j�ł��ؖ�����܂����D
���̃��^�A�i���V�X�́C�X�^�`���̎g�p�œ��A�a�̐V�K���ǂ�OR 1.09�i1.02-1.17�j�{�����邱�Ƃ����������̂ł��D
�X�^�`���ʂł́C���o�X�^�`�����v���o�X�^�`���C�V���o�X�^�`�����A�g���o�X�^�`�������X�o�X�^�`���@�̏��ɃI�b�Y�䂪�オ���Ă����̂ŁCtiter-dependent�ɔ��ǂ���ƌ����܂��D
�����āC�N���X�g�[���ł́C���A�a�̐V�K���ǂ�18%�����������ƂɂȂ�܂��D
��͂�C�K�v�Œ���̖�܂�p����̂��C�X�^�`���̐������g�p�@�ƌ����܂��D
 �������b�͕����Ă����C�t�B�u���[�g�͎g��Ȃ��@�i�ŏI�X�V2012/8/28�j �������b�͕����Ă����C�t�B�u���[�g�͎g��Ȃ��@�i�ŏI�X�V2012/8/28�j
�����ُ�ǂŗp�������܂ɂ͂��܂��܂��̂�����܂����CLDL�R���X�e���[���������ꍇ�ɂ̓X�^�`���C�������b�������ꍇ�ɂ̓t�B�u���[�g�n���p�����邱�Ƃ���ʓI���Ǝv���܂��D
���{�����d���w��̓����d���������\�h�K�C�h���C��2007�N�łł��C���X�N�̐��Ɋ�炸150mg/dL������ڕW�Ɏ��Â���悤�ɏ�����Ă��܂��D
�ł́CLDL�R���X�e���[�����������b�������ꍇ�́C�ǂ�������悢�̂ł��傤���H
�������b�������ƁC�S���ǎ����͑�����̂��H
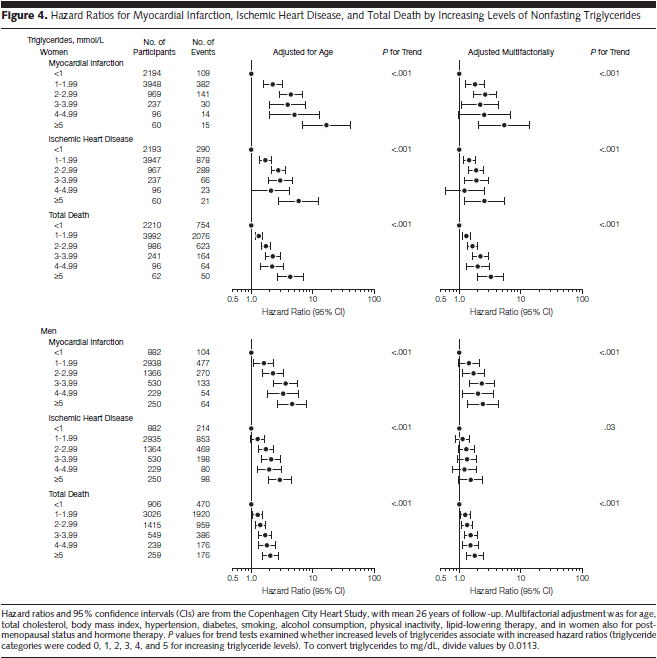
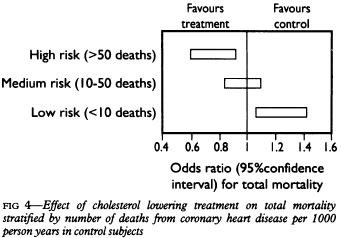
�ߔN�̍ł��傫�ȃR�z�[�g�����iJAMA 2007;298:299�j�ł́C���������b���ǂ͈ꌩ�S���ǎ����̃��X�N�ƂȂ��Ă����Ƃ����f�[�^�ł��D
Fig.4�ʂɌ���ƁC�m���ɂ����ǂ߂܂��D
�������C���ӂ��Ȃ���Ȃ�Ȃ��̂́C����͋��̒������b��1mmol/L�i��88.5mg/dL�j�����̐l����ɂ��čl�����ꍇ�ł��D
���̏ꍇ�C���{�l�ň�ʓI�ɑ���150�`300mg/dL�i1.7�`3.4�j�O�キ�炢���l����ƁC���ϗʂŒ�����ɁC�S�؍[�ǁC�������S�����C�����S�̂������HR
2�`2.5�{���x�̃��X�N������Ɠǂ߂܂��D
�Ƃ��낪�C������C1�`1.99mmol/L�i88.5�`177mg/dL�j����ɍl�����Ƃ�����C150�`300mg/dL�i1.7�`3.4�j�O��̐l�́C���X�N�������X���ɂ��邩���m��܂��C�L�ӂƌ�����قǂ̍��͂Ȃ��Ȃ�܂��D
����ǂ��ɒu�����ɂ���Č��ʂ��ς��͓̂��R�ł����Cmajority����ɒu�����C�����̒�X�N�̏W�c�Ɋ��u�������l�����ꍇ�C���͑O�҂ɂ���̂������I���Ǝv���܂��D
�܂��C�S�̂̌X���́C�j���Ƃ��C�ǂ̃A�E�g�J���ł��L�Ӎ����t���Ă��܂����C�����1mmol/L������5mmol/L�i442.5mg/dL�j�ȏ�̋ɒ[�Ȑl�B�������܂܂�Ă��邩��ŁC��������������C�L�Ӎ����o�Ȃ��Ȃ�\��������܂��D
����ł��C1mmol/L�����Ɣ�r������2�`2.5�{�̃��X�N�Ƃ����͍̂����̂ł͂Ȃ����Ƃ̔��_�����邩���m��܂���D
�{������26�N�Ԃ̊ώ@�����ŁC���̊ԁC�S�؍[�ǂ�13%�C�������S������25%�C�����S��56%�N�����Ă���C�����N���ɒ����ƁC���ꂼ�ꂨ�悻0.5%�C1%�C2%�ɂȂ�܂��D
���{�l�ł̐S�؍[�ǂƋ������S�����̔��Ǘ��́CMEGA study�iLancet 2006;368:1155�j�̑ΏƌQ�ł݂�ƔN��0.16%��0.5%�ł�����CJAMA�̌����̊��҂̔����ȉ��ł��D
�ł�����C2�`2.5�{�ƌ����Ă��C����قǑ傫�ȍ��ɂ͂Ȃ�Ȃ��ƍl�����܂��D
����ɁCJAMA�̌����ɎQ���������҂́C���������҂����C�i���҂���6���ł�����C�����̊댯���q���Ȃ��悤�Ȋ��҂ł́C���X�N�͂���ɉ�������̂Ǝv���܂��D
2009�N�ɔ��\���ꂽ���^�A�i���V�X�iJAMA 2009;203:1993�j�ł��C�������b�͐S���ǎ����̃��X�N�ɂȂ�Ȃ��Ǝ�����Ă��܂��D
�����ȊO�̊댯���q�Œ�����̐S���ǎ����ɑ���n�U�[�h���1.37�i1.31-1.42�j�ł������C����������HDL�R���X�e���[���Ɣ�HDL�R���X�e���[���Œ�������ƁC0.99�i0.94�`1.05�j�ɂȂ�C�L�Ӎ����Ȃ��Ȃ��Ă��܂��Ƃ������Ƃł����D
�G�r�f���X���������Ă��܂����C�������b�͐S���ǎ����̊댯���q�Ƃ͂Ȃ�Ȃ��\��������C���ɂȂ�Ƃ��Ă����̊댯���q�قǏd���͂���ׂ��ł͂Ȃ��ƌ����܂��D
���������b���ǂɃt�B�u���[�g�͎g���ׂ����H
���_���猾���ƁC�t�B�u���[�g������́C�����Ƃ��Ďg���ׂ��ł͂Ȃ��Ǝv���܂��D
�X�^�`���o��ȑO�ɍs��ꂽ��������̓t�B�u���[�g��j�R�`���_��p�������̂���ł������C�����𒆐S�Ƃ������^�A�i���V�X�iBr Heart J 1993;69;S42�j�ɂ��C�ꎟ�\�h���Âɂ����Ă͊����������͌������܂����C���S����OR �P.20�i1.0-1.45�j�ŗL�ӂɑ������Ă��܂����iFigure 3�j�D
�����N�ɏo���ꂽ���̃��^�A�i���V�X�iBMJ 1993;306:1367�j�ł��C�����������ɂ�鎀�S�����N��0.1%�̒�X�N�Q�ł́C�R���X�e���[�����Âɂ�肩�����Ď��S�����オ�����Ƃ��w�E����Ă��܂��iFIG 4�j�D
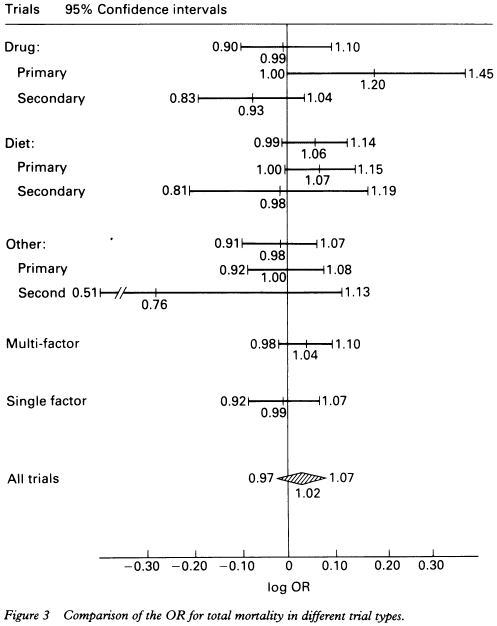 
���̌�s��ꂽfenofibrate�̔�r�I�V���������ł���FIELD trial�iLancet 2005;366:1849�j�ł́Cprimary outcome���������C�x���g��HR 0.89�i0.75-1.05�j�ƗL�Ӎ��������C���S�����L�Ӎ�������܂���ł������CHR 1.11�i0.95-1.29�j�Ƃ�͂葝���X���������܂����D
���������̌����ł́C���A�a���҂�ΏۂƂ��Ă��܂��̂ŁC����ɒ�X�N���҂̏ꍇ�ɂ́C���S���͗L�ӂɑ�������\��������܂��D
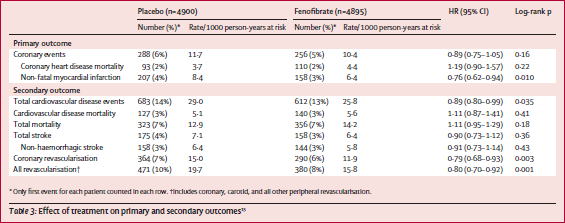
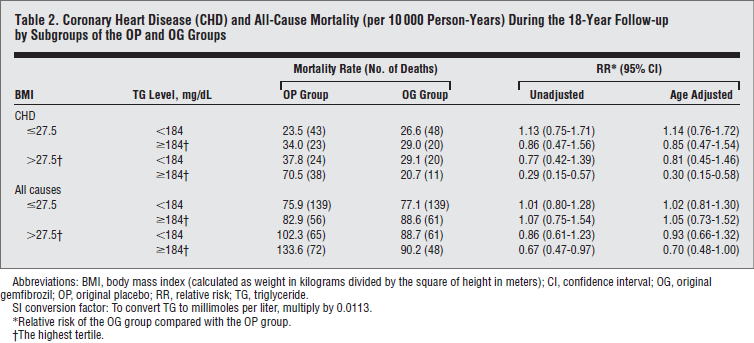
���̌�s��ꂽgemfibrozil��p����Helsinki Heart Study�iArch Intern Med 2006;166:743�j���s���܂����D
18�N�̃t�H���[�ŁC��������S���ǎ�����RR 0.76�i0.59-0.99�j�ƗL�ӂɌ������Ă��܂����C��͂������S��RR 0.92�i0.79-1.08�j�ŗL�ӂɌ��点�Ă͂��܂����D
�������C���̐S���ǎ����̃C�x���g�����́C�T�u��͂ɂ����āCBMI��27.5��TG��184mg/dL�̏ꍇ�Ɍ���0.30�i0.15-0.58�j�ƗL�Ӎ����o�Ă���C����ȊO����얞���҂Ɣ얞���҂ł��������b�l������قǍ����Ȃ��O���[�v�ł͗L�ӂȌ����݂͂��Ă��܂����D
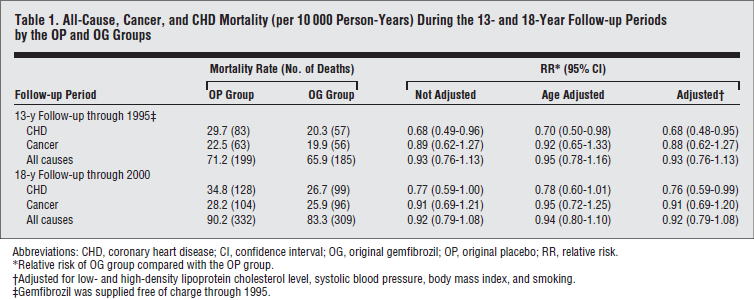
�����āC2010�N�Ƀt�B�u���[�g�̌��ʂ����������V���ȃ��^�A�i���V�X�iLancet 2010;375:1875�j���o�܂����D
���̕ɂ��ƁC�S���ǃC�x���g�C�������C�x���g�C��v���I�������C�x���g�C���������ǍČ��p�C�A���u�~���A�̑����C�Ԗ��ǂ͗L�ӂɌ��炵�܂������C����ŁC�����S�C�S�����C�S���ǎ��C�ˑR���C�ǎ��C�]�����C�S�s�S�͌��炵�܂����ł����D
���̒��ŁC���ɔǎ��͗L�Ӎ��͕t���Ă��Ȃ����̂́C�t�ɑ�����X���������Ă��܂��D

���_�Ƃ��ẮC���������b���ǂ������d���̊댯���q�Ƃ������Ƃ��Ă��C�t�B�u���[�g���g�����ƂŐS���ǎ����͌��邩���m��Ȃ����C���S���ɂ͉e�����Ȃ��C�ƌ����܂��D
���������āC�����̓��{�l�ł́C�������b�l�����������Ƃ��Ă��C�t�B�u���[�g���g�p����Ӌ`�͂Ȃ��ƍl�����܂��D
�X�^�`���ƃt�B�u���[�g�͕��p���ׂ����H
ACCORD�����̃T�u��́iNEJM 2010;362:1563�j�ŁCsimvastatin��fenofibrate�������Ă��C�A�E�g�J�������P���邱�Ƃ��ł��܂���ł����D
���p�ɂ��C����ؗZ���ǂ̔��Ǘ��͔���I�ɏオ��ƌ����Ă���C�X�^�`���ƃt�B�u���[�g�p���邱�Ƃ͊��߂��܂����D
�t�B�u���[�g�͂ǂ������ꍇ�Ɏg���ׂ����H
�ł́C���������b���ǂ͊��S�ɕ��u�ł悢�̂ł��傤���D
�t�B�u���[�g�Ƃ�����͖��p�̒����Ȃ̂ł��傤���D
�����d������̎��_�Œ������b�����܂�d�v�ł͂Ȃ��Ƃ��Ă��C�}���X���ł́C�b������Ă��܂��D
NEJM�̑����iNEJM 2007;357:1009�j�ł́C�������b�l��1000mg/dL�ȏ�ł́C�}���X���̔��\�h�̂��߂Ɏ��Â����ׂ��ƋL����Ă��܂��D
���̍ۂ́C���_�I�ɂ̓X�^�`�������������b�l�̒ቺ���ʂ̍ł��傫���t�B�u���[�g���g�p����̂��ǂ��Ǝv���܂��D
�����āC2012�N�Ɏ����ُ�ǂɑ��鎡�Â��}���X����\�h���邩�ǂ��������������^�A�i���V�X�iJAMA 2012;308:804�j���o�܂����D
���̕ɂ��ƁC16����RCT�ŃX�^�`�����g�p����ƁC�}���X���̔��ǂ͕���4.1�N��RR 0.77�i95%CI 0.62�`0.97�Cp=0.03,
I2=0�j�ɂȂ�܂����D�X�^�`���̓��^�ʂɊւ��Č�������5����RCT�̃��^�A�i���V�X�ł́C���p�ʂ͒����p�ʂƔ�r����RR 0.82�i95%CI 0.59�`1.12�Cp=0.21,
I2=0�j�ƕς��܂���ł����D����ŁC7����RCT�̃��^�A�i���V�X�i����5.3�N�j�ŁC�t�B�u���[�g�̎g�p��RR 1.39�i95%CI 1.00�`1.95�Cp=0.053,
I2=0�j�Ƌt�ɋ}���X���̔��ǂ������錋���ł����D
��͂�C�t�B�u���[�g�͎g���ׂ���ł͂Ȃ��Ƃ�����ł��傤�D
�������b�l�̊�͈͏���ł���150mg/dL��������Ɖz�������x�ł́C�S���呛������K�v���Ȃ��ƌ����܂��D
���������b���ǂ̎���
- ��{�I�Ɏ��Õs�v
- �������b1000 mg/dL�ȏ�͋}���X���̃��X�N�ɂȂ邽�ߎ��ÓK��
- ���Â̓X�^�`���ōs��
- �t�B�u���[�g�͋t�ɋ}���X���𑝂₷�̂Ŏg�p���Ȃ�
- �X�^�`���ƃt�B�u���[�g�p����̂̓����b�g���Ȃ�����ؗZ���ǂ̃��X�N�𑝂₷�̂Ŋ댯
|
 �����R���X�e���[���g�����X�|�[�^�[�j�Q��i�G�[�`�~�uezetimibe�j�@�i�ŏI�X�V2016/4/7�j �����R���X�e���[���g�����X�|�[�^�[�j�Q��i�G�[�`�~�uezetimibe�j�@�i�ŏI�X�V2016/4/7�j
�t�B�u���[�g�C�X�^�`���C�j�R�`���_�ȂǁC�����ُ�ǂ̎��Ö�ɂ͂���������܂����C�����R���X�e���[���g�����X�|�[�^�[�j�Q��ł���[�`�[�A�����{�ł����������悤�ɂȂ�܂����D�R���X�e���[���z����S�������R���X�e���[���g�����X�|�[�^�[�iNPC1L1�j�Ɍ������邱�ƂŁC�_�`������ѐH�����R���X�e���[���̋z����I��I�ɑj�Q���܂��D���ʓI�ɁC�̑��̃R���X�e���[���ܗʂ��ቺ���C�����R���X�e���[���̒ቺ�ɂȂ���̂ł��D
SHARP trial
�ł́C���̃G�r�f���X�́H�Ƃ������ƂɂȂ�̂ł����CLDL�R���X�e���[���������āCHDL�R���X�e���[�����グ���p�͏ؖ�����Ă�����̂́C�S���ǎ������Ǘ��⎀�S���̒ቺ�Ƃ��������Տ��I�ɏd�v�ȃA�E�g�J���ɂ��ẮC2011�N��Lancet��SHARP�Ƃ����Տ������̌��ʂ����\����܂����DCKD���҂ɃX�^�`����ezetimibe�p����ƐS���ǎ���������Ƃ������̂ł������C���̌��ʂ͎����I�ɃX�^�`���̌��ʂ��������̂ł����D�����_�ł́C�ϋɓI�Ɏg���ׂ��Ƃ͌����Ȃ���ł��D
SHARP�iLancet 2011;377:2181�j�y�����_���̔ᔻ�I�ᖡ�z
IMPROVE-IT trial
2015�N1���S���ǃC�x���g��̓\�h�ɂ�����G�[�~�`�u�{�X�^�`���ƃX�^�`���P�ƂƂ��r����IMPROVE-IT�iN Engl J Med 2015;372:2387�j�̌��ʂ����\����܂����D
�S���ǃC�x���g���n�U�[�h��HR 0.936�i95%CI 0.89�`0.99�j�C�S�؍[�ǂ�HR 0.87�i95%CI 0.80�`0.95�j�C�]�[�ǂ�HR 0.86�i95%CI 0.73�`1.00�j�ƌ��������܂������C�S���ǎ��S�Ƒ����S�͌���܂���ł����D
���̌����ɂ͓��A�a���҂�27%�����܂܂�Ă��܂���ł������C���̌��ʂ��ĕč����A�a�w��ł́C2016�N��Position Statement�ŁC�u�����x�̋��x�̃X�^�`�����Âւ̃G�[�`�~�u�̒lj��́C�����x�̋��x�̃X�^�`�����ÒP�ƂƔ�r���āC�t���I�ȐS���ǃx�l�t�B�b�g�������炷���Ƃ�������Ă���CLDL�R���X�e���[����50
mg/dL�i1.3 mmol/L�j�̍ŋߋ}�����nj�Q���N���������҂ƍ����x�X�^�`�����Â��F�e�ł��Ȃ����҂ōl�����邩������Ȃ��v�Ɠ\�h�ɂ����ăX�^�`���ɒlj����鎡�ÂƂ��ăG�[�`�~�u�𐄏����Ă��܂��D
�����C1����RCT�̌��ʂ����ł��̂悤�Ȑ������o�����Ƃ͈ٗ�ł���C���̐������L�ۂ݂ɂ���ׂ��ł͂���܂���D
�܂��̓X�^�`������������g���āC����ł��S�؍[�ǂ̊����̂��銳�҂�LDL-C��100mg/dL�����ɗ}�����Ȃ��ꍇ�̂݃G�[�`�~�u�̎g�p���������܂��i�K���g���Ƃ����킯�ł͂���܂���j�D
���Ȃ낭�̋L�ړ��e�ɊԈႢ�����w�E��������₲�ӌ�����������������́C����C�������܂Ō�A���������D


Copyrights(c)2004- Eishu NANGO
All rights reserved
�֖��f�]��
|